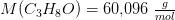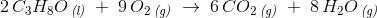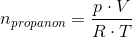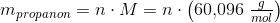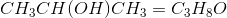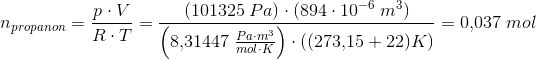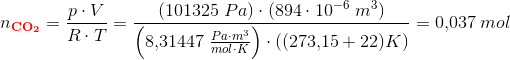Kemi
Propanon
Hej, er der nogle, som kan hjælpe med denne kemiopgave?

Svar #4
27. januar 2016 af Sneharusha (Slettet)
marton:
Men i b ved man ikke hvad p trykket er.
Er proponon ike C3H6O?
Svar #6
27. januar 2016 af Sneharusha (Slettet)
Men her står bare at ar propanon indeholder 6 hydrogen-atommer: https://da.wikipedia.org/wiki/Acetone
Svar #7
27. januar 2016 af mathon
Sorry - jeg læste/tænkte det som propan-2-ol
korrektion:
Forbrænding af acetone 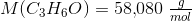
a)
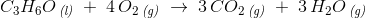
c)
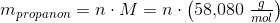
Svar #8
27. januar 2016 af Sneharusha (Slettet)
Det gør intet :)
Men hvordan finder jeg ud af hvad n er? I forhold yil idealgasligningen kender jeg ikke trykket? Skal jeg bare sætte trykket til 1 atm?
Svar #12
27. januar 2016 af Sneharusha (Slettet)
I sidste opgave skal man svarer hvilken masse af propan det svarer til. Tror du de mener propranon?
Svar #14
27. januar 2016 af mathon
C3H6O+ 3O2 -> 2 CO + 3 H2O er forkert,
hvilket en hurtig grundstofatomoptælling tydeligt viser.
Svar #15
27. januar 2016 af Sneharusha (Slettet)
Det var ikke det jeg mente. Jeg tænkte noget og skrevet noget helt andet, men
CH2H5OH + 3O2 -> 2CO2 + 3H2O
Er meget sikker på det er rigtigt.
Skriv et svar til: Propanon
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.