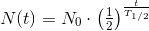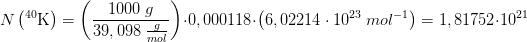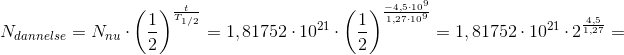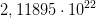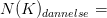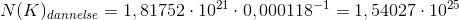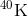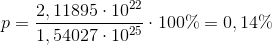Fysik
Kalium-40
Håber nogen kan hjælpe med disse opgaver :-)
I dag udgøres 0,0118% af naturlig kalium af det radioaktive Kalium-40 som halveres på 1,27*109 år
Resten er kalium-39 der er stabilt
a)Hvor mange K-40 kerner er der i 1 kg kalium?
b)Hvor mange K-39 kerner er der i 1 kg kalium?
c)K-40 kan henfalde ved elektronindfangning eller beta- opskriv de to kernereaktioner.
d)Den ene af disse kernereaktioner forklarer, hvorfor der er 0,93% Ar i luften hvilken af dem er det?
e)Hvor mange % udgjorde K-40 ved jordens dannelse for 4,5·109 år siden?
Svar #2
10. september 2014 af Heptan
Der er
n(K-40) = 0,0118 % * n(K)
hvor n(K) er stofmængden af kalium i 1 kg kalium, og n(K-40) er tilsvarende for K-40.
n(K) = m/M = 1000 g/(39,0983 g/mol) = 25,577 mol
Således er stofmængden af K-40 kerner følgende:
n(K-40) = 0,0118 % * 25,577 mol = 0,003018086 mol
Så mange er der.
Svar #3
10. september 2014 af Heptan
b)
Forudsat at der kun er de to isotoper er antallet af K-39 kerner givet ved
n(K-39) = n(K) - n(K-40)
Skriv et svar til: Kalium-40
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.