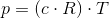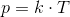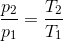Fysik
idealgasligningen
Nogen, der kan hjælpe med denne opgave? Det er især a)
Vi ser i denne øvelse på, hvordan trykket varierer i et bildæk, når temperaturen ændrer sig. Trykket i bildæk angives ofte i enheden bar, og vi ser på et dæk, der ifølge bilfabrikanten skal have et tryk på 3,0 bar. Dette er trykket, som det måles af pumpen på en tankstation, og det angiver trykket ud over atmosfærens tryk. Antag, at dækket er pumpet op til det korrekte tryk ved temperaturen
a) Anvend idealgasligningen til at finde en formel for dækkets tryk p ved en vilkårlig temperatur T. Kald rumfanget ved trykket p og temperaturen T for V. Kald det korrekte dæktryk for p0. Antag, at dækkets rumfang er uafhængig af tryk og temperatur.
Anvend idealgasligningen på formen
p*V/T = n*R = konstant
Bemærk, at den færdige formel ikke indeholder dækkets rumfang.
b)På en solskinsdag når dækkets temperatur op på . Beregn dæktrykket.
c)En vinterdag måles dæktrykket på en tankstation til 2,6 bar.
Find temperaturen af luften i dækket.
Svar #3
23. februar 2015 af Ellapigen (Slettet)
kan godt se du har
gjort brugt af n = m/M
og V = densitet/m
(men jeg får ikke det samme..
Svar #4
23. februar 2015 af Andersen11 (Slettet)
#3
Idealgasligingen udtrykker, at brøken pV/T er konstant. Når rumfanget V er uafhængigt af tryk og temperatur, har man derfor
p1·V/T1 = p2·V/T2
hvoraf man får udtrykket i #1
p2/p1 = T2/T1 .
Vis dine mellemregninger, hvis du finder et andet udtryk.
Svar #5
23. februar 2015 af Ellapigen (Slettet)
jeg tænkte:
p*V = n*R
p = m/M * R*T / densitet/m = (m*R*T/M ) / (m/densitet)
men det kan jeg vel ikke bruge?
Svar #6
23. februar 2015 af Andersen11 (Slettet)
#5
Det er da unødigt besværligt. Følg det vink, der er givet i opgaven.
p·V er ikke lig med n·R, men n·R·T .
Svar #7
23. februar 2015 af Ellapigen (Slettet)
Ja, okay.. men så forstår jeg ikke helt opgave b) ?
kan det passe:
101,3*10^3 Pa / p = 237,15 K / 308,15 K
??
Svar #8
23. februar 2015 af Andersen11 (Slettet)
#7
Man kender tryk p1 og temperatur T1 , når dækket er pumpet op på tankstationen.
I b) angives en temperatur T2, og man kan så beregne det tilhørende tryk p2 . Du har udeladt talværdierne i #0, men de er vel givet i din opgavetekst.
Svar #9
23. februar 2015 af Ellapigen (Slettet)
her er den..
jeg får opgave b til at være 457.124,81 Pa
dog er jeg usikker på om det er helt rigtigt..
Svar #11
23. februar 2015 af Ellapigen (Slettet)
4,05 * 10^3 Pa / p = 273,15 K/ 308,15 K
og så trykket isoleret.. 4,05 * 10^3 Pa er dækkets og luftens tryk..
Svar #12
23. februar 2015 af Andersen11 (Slettet)
#11
På tankstationen: p1 = 1 atm + 3,0 bar = 1,013·105 Pa + 3·105 Pa = 4,013·105 Pa .
T1 = 15 C = 273,15 K + 15 K = 288,15 K
På solskinsdagen: T2 = 35 C = 273,15 K +35 K = 308,15 K
Derfor: p2 = p1 · (T2/T1) = 4,013·105 Pa · (308,15/288,15) = 4,292·105 Pa = 1,013·105 Pa + 3,279·105 Pa
Dæktrykket ud over atmosfærens tryk er derfor 3,28 bar .
Svar #13
23. februar 2015 af Ellapigen (Slettet)
okay, havde ikke set den information med 15 grader celcius..
Svar #14
23. februar 2015 af Ellapigen (Slettet)
i c) er jeg i tvivl om trykket på 2,6 bar er inkluderet atmosfærens tryk?
Svar #15
23. februar 2015 af Andersen11 (Slettet)
#14
Opgaven definerer dæktrykket som trykket ud over 1 atm. Når dæktrykket måles til 2,6 bar, er trykket i dækket
p2 = 1 atm + 2,6 bar .
Svar #16
23. februar 2015 af mathon
Opgavetekstcitat:
"…trykket, som det måles af pumpen på en tankstation, angiver trykket ud over atmosfærens tryk."
Svar #19
23. februar 2015 af Andersen11 (Slettet)
#17
Så er atmosfærens tryk jo netop ikke inkluderet i det dæktryk, som pumpen viser. Se #15.