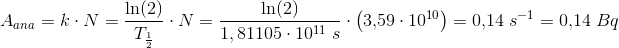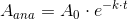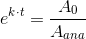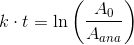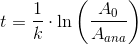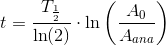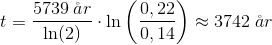Fysik
A 9. Kulstof 14 datering spørgsmål C HJÆLP
C3+- ioner transporterer elektrisk ladning gennem analysatoren med strømstyrken 38μA.
a) Hvor mange C3+-ioner passerer gennem analystoren i løbet af 2,0 minutter?
Resultat: 9.48* 1015 stk.
En meget lille brøkdel af de analyserede ioner er 14C-ioner. Resten kan antages at være 12C-ioner. Man kan derfor regne med at massen af en C3+-ion er 12.0u. I løbet af 2.0 minutter registreres 6.7*103 14C-ioner.
b) Hvor mange 14C-ioner indeholder 1.00g af carbon i tøjet?
Resultat: 3.54*1010 stk/g
14C er β- -radioaktivt med en halveringstid på 5739 år. Aktiviteten fra 1.00g carbon i tøjet på grund af 14C henfald var 0.22Bq da tøjet blev fremstillet.
c) HVOR LÆNGE ER DET SIDEN, AT TØJET BLEV FREMSTILLET?
Det er spg. c jeg er i tvivl om..
Håber der er nogle der kan hjælpe :)
Mvh
Svar #1
25. maj 2015 af mathon
a) Hvor mange C3+-ioner passerer gennem analystoren i løbet af 2,0 minutter?
Resultat: 9,36·1015 stk.
b)
1 g carbon indeholder
af 14C:
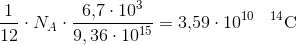
Svar #2
25. maj 2015 af D9 (Slettet)
Tak, men min lommeregner giver mig stadig det andet svar..
Ved du hvordan man regner opgave c?
Svar #4
25. maj 2015 af D9 (Slettet)
Ved godt det lyder lidt dumt, men hvordan fik du 5730 år til sekunder? (altså T1/2)
Svar #5
25. maj 2015 af D9 (Slettet)
Det er lige meget, har fundet ud af det :) Mange tak for hjælpen!!
Skriv et svar til: A 9. Kulstof 14 datering spørgsmål C HJÆLP
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.