Bioteknologi
Syre-base og titrering
Hej! Har fået disse spørgsmål spørgsmål..
1. Hvordan kan det være at jo mere en syre bliver fortyndet, jo mere agerer den som en stærk syre?
2. Hvordan kan det være at når en syre har en lav pKs, er den stærk?
Svar #1
14. marts 2016 af Heptan
1. Stærke syrer dissocierer i høj grad. Når en svag syre bliver fortyndet er det mere sandsynligt at den afgiver en proton end at den korresponderende base optager en. Det skyldes Le Chateliers princip, idet ligevægten
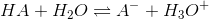
forskydes mod højre ved fortynding.
2. Med syrestyrkeeksponenten pKs kan man associere en ligevægtskonstant Ks, som fortæller hvor ligevægten er forskudt. Små pKs-værdier giver store ligevægtskonstanter, som betyder at ligevægten er forskudt mod højre, dvs. en høj dissociationsgrad.
Svar #2
15. marts 2016 af mathon
2. Hvordan kan det være at når en syre har en lav pKs, er den stærk?
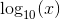 er en voksende funktion
er en voksende funktion
hvoraf:
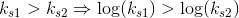
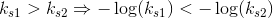
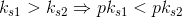
Svar #3
15. marts 2016 af mathon
1. Hvordan kan det være at jo mere en ikkestærk syre bliver fortyndet, jo mere agerer den som en stærk syre?
der gælder Ostwalds fortyndingslov:
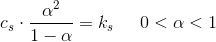 hvor
hvor 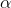 er dissocieringsgraden
er dissocieringsgraden
hvor 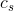 og
og 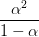 er omvendt proportionale.
er omvendt proportionale.
Mindskes 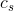 , øges
, øges 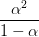 , hvilket kun kan ske, når
, hvilket kun kan ske, når 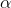 øges.
øges.
Med andre ord:
Når den ikkestærke syre fortyndes, øges dens protonering.
Svar #4
16. marts 2016 af LouisSMW (Slettet)
Kan spørgsmål 2 ikke besvares med noget som omhandler halvækvivalenspunktet?'
Og tak
Skriv et svar til: Syre-base og titrering
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.

