Kemi
Syre og base
Hej SP
Jeg skal afgøre om disse salte opløst i vand giver en neutral, sur eller basisk opløsning samt bruge Brønsteds definition for baser og syrer.
NaNO3
CH3COONa
KCl
K2CO3
NH4Cl
NH4NO3
derudover har jeg et andet spg: Kan salt optræde som syre eller base i vandig opløsning?
Svar #3
16. oktober 2014 af SSunshine (Slettet)
Hvordan ved man om stoffet er neutralt, surt eller basisk? og hvilke stoffer er korresponderende syre-basepar med hinanden samt hvilke optager/afgiver en hydron?
NaNO3 er neutralt fordi der dannes en stærk syre og en stærk base, ikke? men jeg har svært ved at forstå resten.
Svar #4
16. oktober 2014 af mathon
NO3- er neutralt, fordi den er syrerest af en stærk syre pKb = 15,32
Cl- er neutralt, fordi den er syrerest af en stærk syre pKb = 21
CH3COO- er svagt basisk, fordi den er syrerest af en svag syre pKb = 9,25
CO32- er middelstrækt basisk, fordi den er syrerest af en meget svag syre pKb = 3,60
NH4+ er en svag syre, fordi den er korresponderende syre til en svag base. pKs = 9,25
Svar #5
16. oktober 2014 af SSunshine (Slettet)
dvs. at NAOH er den korresponderende base til "syren" H2O
og HNO3 er den korresponderende syre til basen NaNO3
og det er H2O som afgiver en hydron til NaNO3?
så er vand syre og natriumnitrat base, fordi den optager en hydron fra vand?
Håber jeg har forstået det rigtigt.
Svar #7
16. oktober 2014 af Hippocampus (Slettet)
#5
Den korrespondrende syre til basen, OH-, er HOH (H2O)
Det, du skriver ellers, er forkert.
Svar #10
16. oktober 2014 af Hippocampus (Slettet)
Stærk syre + stærk base ---> neutralt salt
Fx:
HCl + NaOH ---> NaCl + H2O
Svar #11
16. oktober 2014 af SSunshine (Slettet)
H2O (l) + NaNO3 (aq) --> HNO3 (aq) + NaOH (aq)
dvs. at OH- er den korresponderende base til syren H2O. Men plejer der normalt ikke at indgå to korresponderende syre-basepar?
og vand afgiver en hydron til NO3? derfor er vand en syre i følge Brønsteds definition, men er det rigtigt at NO3 optager en hydron? hvis OH- er base, hvad er NO3? fordi NO3 optager en hydron og det er en base i følge definitionen?
Svar #12
16. oktober 2014 af mathon
H2O er en yderst svag syre pKs = 15,74
OH- er en stærk base pKb = -1,74
Svar #13
16. oktober 2014 af SSunshine (Slettet)
Men er det rigtigt at OH- er den korresponderende base til H2O (svag syre). Men plejer der normalt ikke at indgå to korresponderende syre-basepar i en reaktion?
og vand afgiver en hydron til NO3 og bliver derfor HNO3? derfor er vand en svag syre i følge Brønsteds definition, men er det rigtigt at NO3 optager en hydron? hvis OH- er en stærk base, hvad er NO3? fordi NO3 optager en hydron og det er en base i følge definitionen?
Håber jeg kan få hjælp til disse spørgsmål.
Svar #14
16. oktober 2014 af Hippocampus (Slettet)
Nitrat er en yderst svag base med pKb = 15,35
Bemærk at nitrat skrives NO3-
#12: Jeg kan nu ellers kun finde kilder på, at pKb(OH-) = 0
Svar #15
16. oktober 2014 af SSunshine (Slettet)
hvad med svaret til dette spg: Men er det rigtigt at OH- er den korresponderende base til H2O (svag syre). Men plejer der normalt ikke at indgå to korresponderende syre-basepar i en reaktion?
samt: afgiver vand en hydron til NO3-?
Og er dette rigtigt:
NaOH er en stærk base
HNO3 er en stærk syre
H2O er en svag syre
NO3- svag base
og derfor er det en neutral opløsning da vand + salt omdannes til en stærk syre og en stærk base.
H2O+ (l) + NaNO3- (aq) --> HNO3 (aq) + NaOH (aq)
Svar #16
17. oktober 2014 af Heptan
#14
pKa for H2O (som en syre) er 15,74. Og da vand er lige stærk som syre og som base, er pKb for vand også 15,74.
Den korresponderende base for vand (OH-) har altså pKb = 14 - pKa = 14 - 15,74 = -1,74
Tilsvarende har den korresponderende syre for vand (H3O+) pKs = -1,74
http://www.masterorganicchemistry.com/2012/05/17/a-handy-rule-of-thumb-for-acid-base-reactions/
_________________________________________________________________________________
Ofte antager man at pKa for vand er 14,0. Det er under antagelse af at vand er i koncentrationen 1,0 M. Men det er jo sjældent tilfældet.
Når 1 L vand vejer 1 kg har vi:
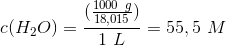
Der er jo en væsentlig forskel. Lad os se hvilken logaritmisk forskel det er:
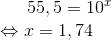
Vi kan også beregne pKa ved vands egendissociation, da vands ionprodukt er Kv = 10-14:
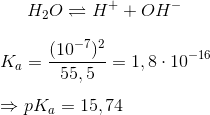
Svar #17
17. oktober 2014 af Heptan
#15
Men er det rigtigt at OH- er den korresponderende base til H2O (svag syre).
Ja, men vand er en yderst svag syre.
Men plejer der normalt ikke at indgå to korresponderende syre-basepar i en reaktion?
Jo, en syre bliver til dens korresponderende base, og en base bliver til dens korresponderende syre (hvis der er tale om en syre/base reaktion).
samt: afgiver vand en hydron til NO3-?
Nej. Jeg vil vove at påstå at reaktionen her er fiktiv:
H2O (l) + NaNO3 (aq) → HNO3 (aq) + NaOH (aq)
... da nitrat er en yderst svag base. Men reaktionen kan forløbe den modsatte retning, dvs.
HNO3 (aq) + NaOH (aq) → H2O (l) + NaNO3 (aq)
Her optager hydroxid en hydron fra salpetersyre (salpetersyre er en middelstærk syre)
Og er dette rigtigt:
NaOH er en stærk base Ja
HNO3 er en stærk syre Nej (middelstærk*)
H2O er en svag syre Nej. Vand er en yderst svag syre. Desuden er vand en amfolyt, dvs. den er også en yderst svag base.
NO3- svag base Nej. Yderst svag base*

og derfor er det en neutral opløsning da vand + salt omdannes til en stærk syre og en stærk base.
H2O+ (l) + NaNO3- (aq) --> HNO3 (aq) + NaOH (aq)
Nej
Svar #18
17. oktober 2014 af SSunshine (Slettet)
Mange tak for hjælpen, men jeg har et sidste spg.
Opgaven lyder: Afgør om disse salte opløst i vand giver en neutral, sur eller basisk opløsning samt bruge Brønsteds definition for baser og syrer.
Og i #1 får jeg at vide at det er en neutral opløsning til det første salt NaNO3
men til sidst i #17 får jeg at vide at det ikke er en neutral opløsniing.
Er blevet forvirret omkring dette.
Svar #19
17. oktober 2014 af SSunshine (Slettet)
Og det her er reaktionen:
H2O+ (l) + NaNO3- (aq) --> HNO3 (aq) + NaOH (aq)
Og jeg skal afgøre om det er en sur, basisk eller neutral opløsning.
Hvilket stof afgiver så en hydron i den overstående reaktion?
Og jeg ved at hydroxid optager en hydron fra saltpetersyre hvis det er den modsatte reaktion, men hvad med til denne reaktion? Hvorfor er det forkert at NO3 optager en hydron fra hydroxid, jeg kan ikke se andre muligheder?
Svar #20
17. oktober 2014 af Heptan
#18
Det har jeg ikke sagt
Hvad har reaktionen med din opgave at gøre?? Det er en meget fiktiv reaktion, jeg har aldrig set den før. Hører den til en anden opgave eller hvad ??
Og det jeg mente i slutningen af #17 var, at
"da vand + salt omdannes til en stærk syre og en stærk base.
H2O+ (l) + NaNO3- (aq) --> HNO3 (aq) + NaOH (aq)" er forkert