Kemi
kemi
nogen der kan hjælpe mig
Svar #2
14. september 2015 af Arccossintan (Slettet)
Når du har afstemt reaktionsskemaet, kender du reaktionsforholdene. Du må først omregne antallet af gram glukose til antallet af mol. Dette gøres på formlen herunder; altså ved at dividere massen med molarmassen:
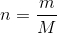
Molarmassen for glukose, kan du slå op.
Du kan nu ved at multiplicere produkternes koefficienter med stofmængden af glukose finde stofmængderne for produkterne og dermed ethanol. Herefter finder du ethanols molarmasse og multiplicere denne med stofmængden og finder således massen, som jeg formoder, at opgaven går ud på. Anvend denne formel:
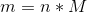
Bemærk at formlen har samme ophav som den første formel - her et det blot massen, som er isoleret i ligningen.
Mvh. Emil
Svar #6
14. september 2015 af hellokitty3
altså jeg ved hvad massen er og moralmassen og så kan jeg divdere de to og får stofmængden men hvordan kommer jeg videre?
Svar #7
14. september 2015 af Arccossintan (Slettet)
Godt, det er korrekt! Find nu antallet af mol glukose. Dette gør du, som jeg forklarede i #1:

Du har altså 0,139 mol. Da glukose og ethanol reagerer i forholdet 1:2 fås den dobbelte stofmængde ethanol, altså:

Omregn nu stofmængden (antal mol) til massen (antal gram):

Altså fås 12,8 g ethanol.
Skriv et svar til: kemi
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.



