Kemi
Kemi hjælp!
Beregn pH i en opløsning af
a. En blanding af 60 mL 0,1 M HCl og 60 mL 0,1 M NaOH
b. En blanding af 60 mL 0,1 M HCl og 40 mL 0,1 M NaOH
c. En blanding af 60 mL 0,1 M HCl og 40 mL 0,5 M NaOH
Aner ikke, hvad jeg skal gøre
Svar #1
04. november 2015 af mathon
a)
lige mange mol HCl og NaOH dvs netutral 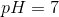
b) og c)
beregn antal overskudsmol af 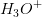 eller
eller 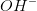 i
i 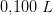 opløsning.
opløsning.
Svar #10
04. november 2015 af Annemarie857 (Slettet)
Hvordan får du det til 1,853? Det kan jeg ikke få det til, når jeg indsætter det
Skriv et svar til: Kemi hjælp!
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.




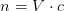
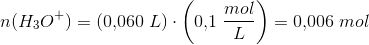
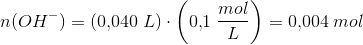
![[H_3O^+]=\frac{0{,}002\; mol}{0{,}100\; L}=0{,}02\; M](https://media.studieportalen.dk/images/equations/L585OLpvCLCNubf6qZIjew==.gif)
![pH=-\log(\left [ H_3O^+ \right ]/M)=-\log(0{,}02)=1{,}7](https://media.studieportalen.dk/images/equations/RBY7gZpnIRtTnNwcCCvPGw==.gif)
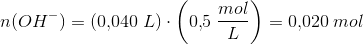
![[OH^-]=\frac{0{,}014\; mol}{0{,}100\; L}=0{,}14\; M](https://media.studieportalen.dk/images/equations/4gwYFiLbdoGaXzTT-ebFxg==.gif)
![pOH=-\log(\left [OH^- \right ]/M)=-\log(0{,}14)=1{,}85387](https://media.studieportalen.dk/images/equations/X1Tg0DGBHl7LFY4J5__PMw==.gif)
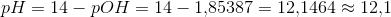
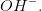
![pOH=-\log(\left [OH^- \right ]/M)=-\log(0{,}14)=0{,}85387](https://media.studieportalen.dk/images/equations/g7JNhwmNe-kC3LZcswaC-w==.gif)