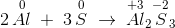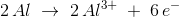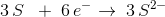Kemi
Redoxreaktion
Jeg har reaktionen Al + S --> Al2S3
Jeg skal redegøre for delreaktioner og oxidationstal. Er dette korrekt:
først afstemmes reaktionen: 2 Al + 3 S --> Al2S3
(eller skrives den således: 2 Al + 3 S --> 2 Al3+ + 3 S2- ?)
Oxidation: 2 Al --> Al23+ + 6 e-
Reduktion: S32- + 6 e- --> 3 S
Oxidationstallet = den interne ladning. Dvs:
Al23+ = III
S32- = II
Svar #1
03. august 2016 af Manu0407 (Slettet)
Og er det korrekt, at AL og S er redoxpar, fordi S optager de elektroner, som Al afgiver?
Svar #2
03. august 2016 af Manu0407 (Slettet)
Mht. oxidationstal:
den samlede stigning skal være lig den samlede reduktion.
Vil det sige, at oxidationstallet for Al = 3*2 --> 6 og for S = -3*2 --> -6 ?
Skriv et svar til: Redoxreaktion
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.