Kemi
Hjælp til kemi C
Jern reagerer med dihydrogensulfat og der dannes dihydrogen (gas) og jern(II)sulfat.
1. Opskriv reaktionsligningen og afstem den.
2. Hvor mange g jern(II)sulfat og dihydrogen dannes, hvis vi bruger 24,5 g jern og 32,6 g dihydrogensulfat?
3. Hvad er hydrogenets volumen ved et tryk på 0,98 bar og en temperatur på 19,7C?
4. Er jern eller dihydrogensulfat den begrænsende faktor?
Svar #2
24. januar 2017 af vSilleBieber (Slettet)
2.
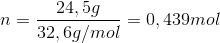
3.
Du anvender formlen:
 p*v=n*R*T, hvor
p*v=n*R*T, hvor
p= 0,98 bar.
n er regnet ovenfor.
T = 19,7.
R = 0,8134472 bar*L/mol*K
Formel skal omskrives, da du gerne vil finde V:
V=(R*T/P)*n
Svar #3
24. januar 2017 af MathAsucks (Slettet)
#22.
3.
Du anvender formlen:
p*v=n*R*T, hvor
p= 0,98 bar.
n er regnet ovenfor.
T = 19,7.
R = 0,8134472 bar*L/mol*K
Formel skal omskrives, da du gerne vil finde V:
V=(R*T/P)*n
2) er ikke korrekt, du beregner ikke mængden (g) af hhv. jern(II)sulfat og dihydrogen der dannes.
Skriv et svar til: Hjælp til kemi C
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.






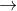 FeSO4(aq) + H2(g)
FeSO4(aq) + H2(g)