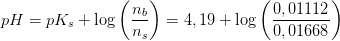Kemi
Syre-base
En mættet opløsning af benzoesyre i vand ved 25 grader celcius indeholder 3,4 g C6H5COOH pr. liter.
a) Vis, at i den mættede opløsning har benzoesyre en koncentration på 0,0278 M.
b) Beregn pH i den mættede benzoesyreopløsning. pKs = 4,19
Til 400 mL af den mættede benzoesyreopløsning sættes nu NaOH(s) indtil al syren netop er forbrugt (ækvivalenspunktet er nået).
c) Opskriv et reaktionsskema for den proces, der finder sted.
d) Beregn, hvor mange gram NaOH der forbruges ved processen.
e) Beregn pH i den dannede opløsning. Der kan ses bort fra ændringer i rumfanget ved tilsætning af NaOH.
Disse 400 mL opløsning (fra spørgsmål e) blandes nu med 600 mL af den oprindelige, mættede benzoesyreopløsning.
f) Beregn pH i denne pufferopløsning.
Mine bud)
a) C = 0,0278 mol/L
b) pH = 2,87
c) C6H5COOH(aq) + NaOH(s) --> C6H5COONa(aq) + H2O(l)
d) ?
e) ?
f) ?
Nogen som vil hjælpe mig med opg. d, e og f?
Svar #1
08. oktober 2014 af mathon
d)
der forbruges
n(NaOH) = n(C6H5COOH) = (0,400 L) · (0,0278 mol/L) = 0,01112 mol
beregn masen heraf.
Svar #4
08. oktober 2014 af mathon
e)
Opløsningen indeholder 0,01112 mol C6H5COO- (svag base) i 400 mL.
[C6H5COO- ] = (0,01112 mol) / (0,400 L) = 0,0278 M
pH = 7 + (1/2)•(pK_s + log(cb))
Svar #7
08. oktober 2014 af Hippocampus (Slettet)
Jeg ved godt, at spørgsmålet i e) henviser til, at man skal beregne pH i opløsningen uden at tage højde for venstre side af reaktionen, men principielt er det vel en buffer?
Svar #8
08. oktober 2014 af Hippocampus (Slettet)
Skriv et svar til: Syre-base
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.