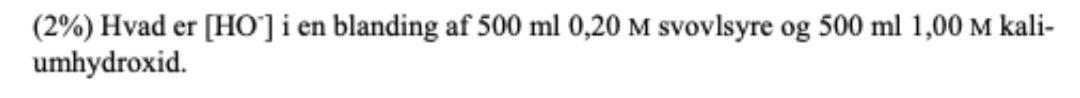Kemi
koncentration
09. januar 2022 af
Lise123Lise
-
Niveau: A-niveau
n=c*V
start: n(OH-)=0,500 mol og x n(H+) = 0,200 mol
0,500 - 0,200 = 0,300 mol
overskud: n(OH-) = 0,300 mol i 1000 mL
Vedhæftet fil: Skærmbillede 2022-01-09 kl. 12.05.12.png
Skriv et svar til: koncentration
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.