Kemi
Kemi
14. november 2016 af
SophieSamantha (Slettet)
-
Niveau: Universitet/Videregående
Tak på forhånd! :)
1) En natriumhypokloritopløsning V(NaClO)=0,650 L og C(NaClO)=0,800M tilsættes fortyndet saltsyre, V(HCl)=0,950L og C(HCl)=0,580M. Beregn massen af klorgas der kan dannes.
M(CL)=35,453 g/mol, M(NaClO)=74,442 g/mol og M(HCl)=36,461 g/mol.
Svar #3
14. november 2016 af SophieSamantha (Slettet)
Jeg kan ikke helt se det, jeg kan ikke finde ud af at beregne massen, det er ikke reaktionsskema jeg er ude efter :c
Skriv et svar til: Kemi
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.




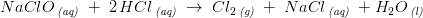
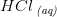 er den 'begrænsende faktor'
er den 'begrænsende faktor'