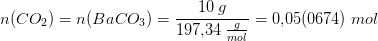Kemi
Trykberegning
Hej jeg har denne opgave:
Ved opvarmning af BaCO3(s) til 1360 C nedbrydes det og der dannes BaO(s) og CO2(g)
10g BaCO3(s) kommes i et lufttomtrum med volumen 3 L. beholderen opvarmes til 1400 C. -
a) Beregn trykket af CO2(g) i beholderen ved 1400 C.
Men hvordan gør jeg? der er jo en formel : p= n*R*T / V
så jeg tænker at jeg skal have n for CO2.. men hvordan finder jeg den?
så vidt jeg kan se, så reagerer BaCO3(s) -> BaO(s) + CO2(g) 1:1:1
BaCO3(s) M 197.311 g*mol n 0.050681 mol. m 10 g
BaO(s) M 153.32 g* mol
CO2(g) M 44.009 g*mol
Så Hvordan finder jeg n CO2(g) så jeg kan finde trykket på CO2?
Skriv et svar til: Trykberegning
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.