Fysik
termodynamik HJÆLP.
er der nogen der kan hjælpe med opgave 2.3. jeg har beregnet opgave 2.2 til 3,556.
og ved jeg har 500g som skal omregnes til mol.
formelen som jeg har fundet fra til er 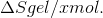
jeg har vedhæftet selve opgaven.
Svar #1
04. april 2015 af GalVidenskabsmand (Slettet)
Der er 500 g stivelse, som har molmassen 40*106 g/mol. Stofmængden kan så beregnes til
n = m/M
n = 500 g / 40*106 g/mol = 12,5*10-6 mol
Så er det vel bare at dividere ΔgelS med n:
ΔgelSm = ΔgelS / n
Svar #2
06. april 2015 af isabellaKramer (Slettet)
Hej hans0099
Kan du så hjælpe mig med opgave 2,2 evt???
Svar #3
06. april 2015 af GalVidenskabsmand (Slettet)
Jeg skrev sammen med Hans tidligere i dag. Du kan lige få en kopi af en besked, jeg sendte til ham:
Udtrykket for Qgel:
Qgel = 500g * (∫7080 (0,8/10)*(T - 70)*dT + ∫8090 (0,8 - (0,8/10)*(T - 80))*dT)
Entropien finder vi ved at dividere med T i integralerne (da ΔS = ∫ dQrev/T )
ΔSgel = 500g * (∫7080 (0,8/10)*(1 - 70/T)*dT + ∫8090 (0,8/T - (0,8/10)*(1 - 80/T))*dT) =
500 * ( [0,08T - 0,08 * 70*ln(T)]7080 + [0,8*ln(T) - 0,08T + 0,08*80*ln(T)]8090 )
Som jeg får til 50,1 J/K. Vi dividerer så med 12,5*10-6 mol og får
ΔgelSm = 4,01*106 J/(K*mol)
Et meget stort tal. Måske skal det være stort på grund af, at stivelsesmolekylerne er så kæmpestore. Der er jo kun 12,5*10-6 mol, selvom det vejer 500g, dvs., at 1 mol stivelse ville veje 500g/(12,5*10-6) = 40 tons.
Svar #4
06. april 2015 af isabellaKramer (Slettet)
Svar #6
06. april 2015 af isabellaKramer (Slettet)
Jeg er nu ikke enig i din udregning af Q på. Jeg har benyttet mig af formlen 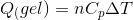 . og det har jeg fået til at give
. og det har jeg fået til at give 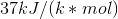 . Man kan også udregne den ved at sige
. Man kan også udregne den ved at sige 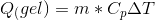 , her er
, her er 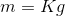 og
og 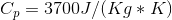 . Begge måder giver det samme resultat. Og det var for en isobarisk proces.
. Begge måder giver det samme resultat. Og det var for en isobarisk proces.
Svar #7
06. april 2015 af isabellaKramer (Slettet)
Entropien udtrykket du også i enheden, så vidt jeg mener og kan se i min lille fysik bibel er det så ikke 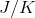 ?
?
Svar #8
13. april 2015 af Mortenkat (Slettet)
hvordan fik du opgave 2.2 til at give 3,556 isabella? fik det nemlig til 21.6 og opgave 2.1 til 8000 :)
Svar #10
08. maj 2015 af Heptan
#6
Det er forkert, cp, ex er jo ikke konstant. Man kan se på grafen at den varierer i temperaturintervallet, og den varierer mellem 0 og 0,8 Jg-1K-1, så derfor er man nødt til at konstruere en type funktionsforskrift og bestemme integralet.
Værdien 3,7 kJ kg-1K-1 er jo for opvarmning af risene, og ikke for gelatinering af risene. Man kan tænke lidt på det som en faseovergang, som altså kræver ekstra energi. Faseovergangen har ikke ét smeltepunkt, fordi stivelsesmolekylerne ikke er identiske, så derfor skal man se på hele temperaturintervallet 70 ºC - 90 ºC.
Se også https://www.studieportalen.dk/forums/thread.aspx?id=1589755
Skriv et svar til: termodynamik HJÆLP.
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.

