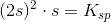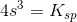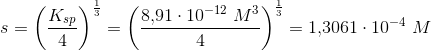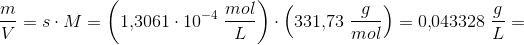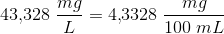Bioteknologi
sølvchromats opløselighed i vand
27. september 2015 af
MartinMosgaard (Slettet)
-
Niveau: A-niveau
Opgave 22 – Anvend opløselighedsproduktet i tabel 4 for C til at beregne stoffets opløselighed i vand ved 25 grader. Er sløv(l)chromat lettere eller tungere opløseligt i vand end sløv(l)chlorid?
Hvordan finder jeg sølvchromats opløselighed i vand?? Jeg har prøvet i godt 30 min, men jeg sidder fast :/
Skriv et svar til: sølvchromats opløselighed i vand
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.









![\left [ Ag^{+} \right ]=2\cdot \left [ Ag_2CrO_4 \right ]=2s](https://media.studieportalen.dk/images/equations/qaRm29QbnEU9G_aFQ1SL0Q==.gif)
![\left [ Cr{O_4}^{2-} \right ]= \left [ Ag_2CrO_4 \right ]=s](https://media.studieportalen.dk/images/equations/U4eeh07ZUIxSDPNvhB6vtw==.gif)
![\left [ Ag^{+} \right ]^{2}\cdot \left [ Cr{O_4}^{2-} \right ]=K_{sp}](https://media.studieportalen.dk/images/equations/ekuFNfb8_ojWE5lCQ4uDJw==.gif)