Kemi
BEREGNING
03. maj 2021 af
Østergaard1234 (Slettet)
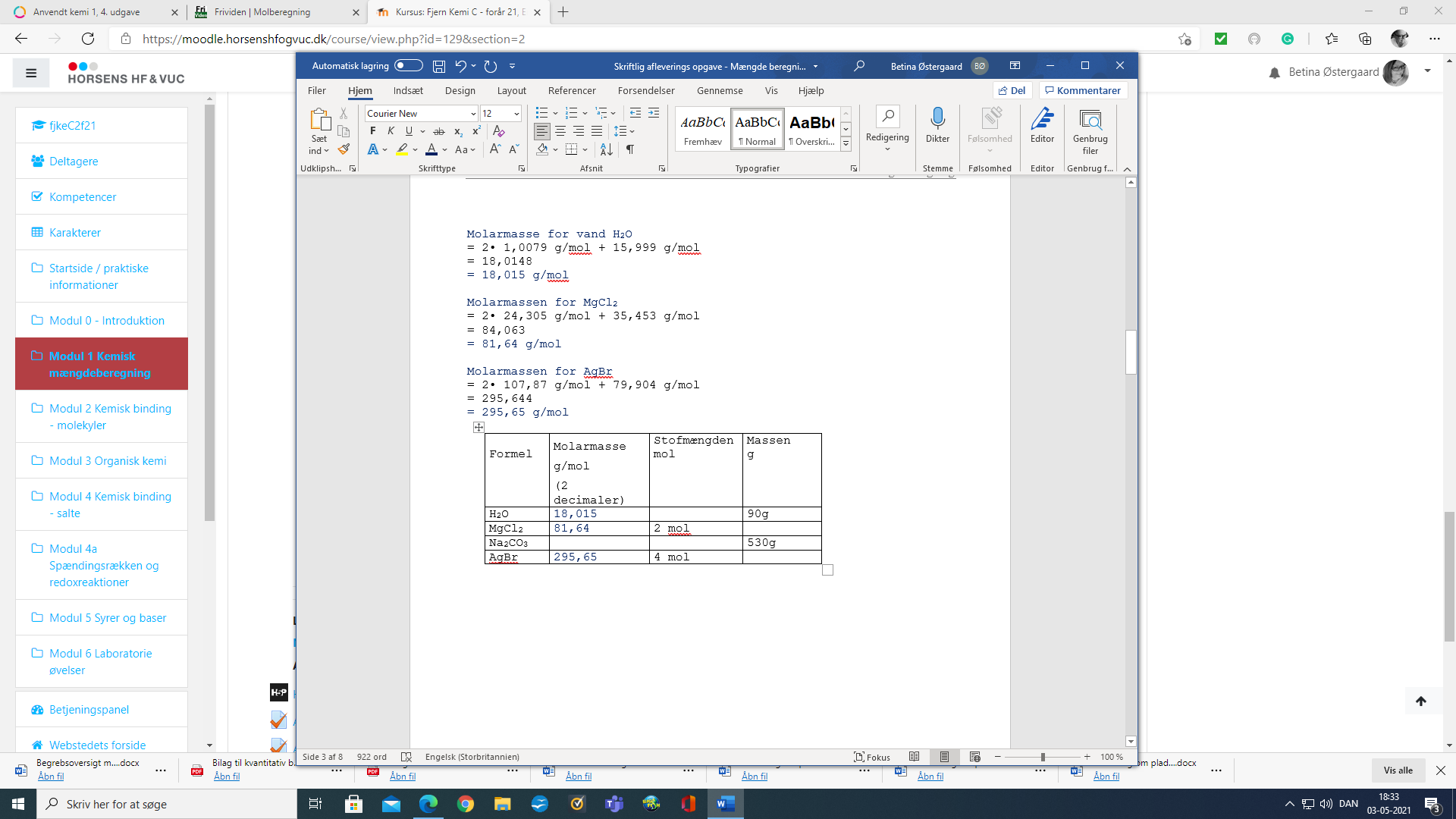
Håber der findes en som vil give mig en forklaring på, hvor resten skal beregnes
Se venligst vedhæftede skærmbillede
Jeg har regnet lidt på det, men så gik klappen ned
Vedhæftet fil: Skærmbillede (355).png
Skriv et svar til: BEREGNING
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.