Kemi
Side 2 - reaktionshastighed
Svar #21
19. oktober 2014 af paaske1 (Slettet)
Jeg mener: Hvordan kan man bestemme, hvilken orden det er ud fra en graf?
Svar #22
19. oktober 2014 af Hippocampus (Slettet)
En reaktion af 0. orden kan beskrives ved
[A] = -k·t + A0
og dermed ved en lineær regression af de indsamlet dataene.
Tilsvarende kan en reaktion af 1. orden beskrives ved en eksponentiel funktion.
Reaktioner af 2. orden kan beskrives ved en reciprok funktion.
Svar #24
19. oktober 2014 af Heptan
Se #13 igen
Hvis eksponenten er 1, så er det en førsteordensreaktion. Hvis den er 2, så er det en anden ordens reaktion.
Svar #25
20. oktober 2014 af paaske1 (Slettet)
I #13 står der, at forskriften svarer til
![\frac{1}{v}=\frac{1}{k}\cdot [I^-]^-^y](https://media.studieportalen.dk/images/equations/_DNFA3Z_J_924iEev4IChA==.gif)
hvordan det?
Svar #26
21. oktober 2014 af Heptan
Hvis  er et mål for reaktionshastigheden v, så er
er et mål for reaktionshastigheden v, så er 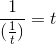 et mål for den reciprokke reaktionshastighed
et mål for den reciprokke reaktionshastighed
Altså kan man antage at 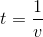
_______________________________________________
I b. er den en fordel at gøre som #22, fordi så kan den samlede orden findes. Hvis man finder, at iodid er af første orden, og at den samlede orden er 2, så kan man altså slutte at reaktionen er af første orden med hensyn til persulfat.
Skriv et svar til: reaktionshastighed
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.

