Kemi
Reaktionshastighed
13. december 2015 af
Pizzaglad (Slettet)
-
Niveau: B-niveau
Hej, er der nogen der kan hjælpe mig med at besvare dette spørgsmål:
Forklar forskellen på at bestemme reaktionshastigheden ud fra omdannelsen af reaktanter eller ud fra dannelsen af produkter.
På forhånd tak!! :)
Forklar forskellen på at bestemme reaktionshastigheden ud fra omdannelsen af reaktanter eller ud fra dannelsen af produkter.
På forhånd tak!! :)
Skriv et svar til: Reaktionshastighed
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.


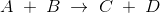
![v=-\frac{\mathrm{d} \left [ A \right ]}{\mathrm{d} t}=-\frac{\mathrm{d} \left [ B \right ]}{\mathrm{d} t}=k\cdot \left [ C \right ]^{x}\cdot \left [ D \right ]^y](https://media.studieportalen.dk/images/equations/5biaIc67uBKUHMF9Cpvd-Q==.gif) reaktanternes koncentration er aftagende.
reaktanternes koncentration er aftagende.![v=\frac{\mathrm{d} \left [ C \right ]}{\mathrm{d} t}=\frac{\mathrm{d} \left [ D \right ]}{\mathrm{d} t}=k\cdot \left [ C \right ]^{x}\cdot \left [ D \right ]^y](https://media.studieportalen.dk/images/equations/ymIYIR7AtSsqgtX5eZeB6w==.gif) produkternes koncentration er voksende.
produkternes koncentration er voksende.