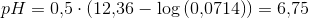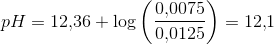Kemi
pH-beregning
Hej! Jeg har siddet og prøvet på at regne en opgave i længere tid, og føler at jeg bruger den rigtige metode, men får hele tiden det forkerte resultat, håber nogen kan hjælpe.
2,84 g Na2HPO4 opløses i vand til ialt 100,0 mL
a) beregn opløsningens molaritet = dette har jeg beregnet til 0,2387 mol/L via først n= m/MV, dernæst C=n/V.
b) til denne opløsning sættes 100,0 mL 0,100 M HCl. Beregn pH efter tilsætningen.
- Her vil jeg gerne bruge puffer ligningen pH = pKs +log([nb]/[ns]) => pH = -7 + log(0,02387/0,01), men dette giver ikke det rigtige da jeg får -6,62, men det burde give 7,2?
c) til opløsningen i spørgsmål (a) sættes 75,0 mL 0,100 M NaOH. Beregn pH efter tilsætningen.
Svar #2
08. februar 2016 af iamjustadreamer (Slettet)
Det giver ikke rigtig mening, da C´eren ifølge min facitliste skal give 12,2 ? :D.
Skriv et svar til: pH-beregning
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.


![pH=0{,}5\cdot \left ( pK_{s3}-\log\left (\left [HP{O_4}^{2-} \right ]/M \right ) \right )](https://media.studieportalen.dk/images/equations/_-f5u5lXfhOuw_4d7SCaGQ==.gif)