Kemi
Spaltning af hydrogenperoxid (reaktionshastighed)
Hej SP, håber at kunne få lidt hjælp med denne opgave:


Jeg mener, at det er noget med, at man ser på "hvis jeg øger koncentrationen af dette så meget, ændrer hastigheden sig så meget" og så kan man vist konkludere, hvilken orden det er, men jeg kan bare ikke helt huske, hvordan det fungerer.
Mange tak for hjælpen!
Svar #1
24. februar 2016 af Soeffi
#0
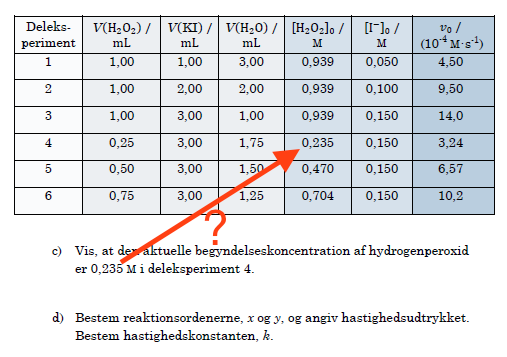
d) Du skal se på de steder hvor [H2O2]0 holdes konstant lig med 0,939 M, og se hvordan starthastigheden varierer med startkoncentrationen af I-. Derefter skal du se på de steder, hvor [I-]0 er konstant lig med 0,150M og se på, hvordan starthastigheden varierer med startkoncentrationen af H2O2.
Svar #3
24. februar 2016 af Hrylla (Slettet)
#1
Tak fordi du gider at hjælpe!
Jeg satte [I-] /M ind som mine x-værdier og hastigheden ind som y-værdier i Excel, og bad den så om, at give mig en potensfunktion. Den gav mig ligningen y=101,59 · x1,0,79, betyder det så, at den del er en første ordensreaktion?
Svar #5
24. februar 2016 af Hrylla (Slettet)
#4
Kan du også hjælpe mig med c)?
Jeg har regnet at H2O2's stofmængde er 0,007827659199 mol. Tænker, at jeg nok ikke skal have fat i c = n/v, da denne vil give den formelle stofkoncentration.
Jeg har sat op:

Er jeg overhovedet på rette spor her? Og hvis jeg er, hvordan kommer jeg videre?
Svar #6
24. februar 2016 af Soeffi
#5
Jeg forstår ikke spørgsmålet. Så vidt jeg kan se fremgår svaret af tabellen!
Svar #7
24. februar 2016 af Hrylla (Slettet)
#6
Ja, jeg synes nemlig også det er forvirrende ^^"
Tænker, at de gerne vil have, at jeg viser beregningen til, hvordan de fik det tal, men er ikke helt sikker på, hvordan jeg skulle gøre det.
Tak for din hjælp alligevel! Kom da noget videre :)
Skriv et svar til: Spaltning af hydrogenperoxid (reaktionshastighed)
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.

