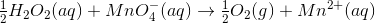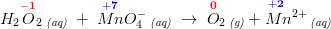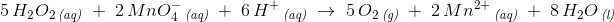Kemi
Reaktion mellem mangang og hydrogen peroxid (redox)
Jeg bøvler lidt med at få den her reaktionsligning til at blive afstemt.
Det er en redoxreaktion i suropløsning mellem hydrogenperoxid og mangan.
Jeg har fundet frem til følgende:
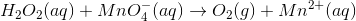
Oxygen har oxidationstallet -I på venstre og 0 på højre
Mangang har VII på venstre og II på højre.
Når jeg vil afstemme ladningen indsætter jeg 3 hydrogenatomer på venstre side, da jeg har en negativ ladningsforskel på -III fra -I til +2 - og så er det så det går galt.
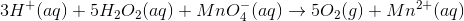
Når jeg tæller oxygen hydrogen for at jeg har 13 på venstre side og ingen på højre
Hvad gør jeg galt?
Skriv et svar til: Reaktion mellem mangang og hydrogen peroxid (redox)
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.