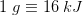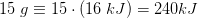Kemi
Kemiske reaktioner
Hej :)
Jeg har brug for hjælp til følgende spørgsmål:
Glucose, also known as 'blood sugar' when measured in blood, has the formula C6H12O6.
a) Write the equation for the combustion og flucose with O2 to give CO2 and H2O.
C6H12O6 + 6 O2 -(kan ikke lave en pil) 6 CO2 + 6 H2O
b) If 3.8 kcal (16 kJ) is released by combustion of each gram of glucosem how many kilocalories are released by the combustion of 1.50 mol of glucose?
MC6H12O6 = 180.156 g/mol
Omregner 3.8 kcal/gram om til mol/g:
3.8 kcal/gram * 180.156 g/mol = 684.59 kcal/mol
1.50 mol * 684.59 kcal/mol = 1026.885 kcal
Som jeg så omregner til kJ:
1026.885*4.184 kJ = 4296.49 kJ
Men så kommer c), som jeg simpelthen ikke kan finde ud af:
c) What is the minimum amount of energy (in kJ) a plant must absorb to produce 15.0 g of glucose?
Tak på forhånd :)
Skriv et svar til: Kemiske reaktioner
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.