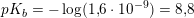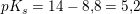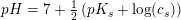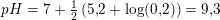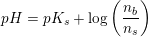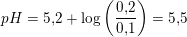Kemi
PH
En liter 0,100 M HCl opløsning tilsættes 0,300 mol pyridin uden rumfangsændring. Hvad bliver pH i blandingen?
kb = 1.6 * 10^-9
Mit bud ses i vedhæftede billede..
Er der nogen der kan spotte fejlen? Løsningen er 5.51
Svar #1
29. maj 2017 af mathon
Der er overskud af pyridin, som er en base, hvorfor pH ikke kan være 5,51.
Svar #4
29. maj 2017 af Unintended96 (Slettet)
Min lærer har angivet svaret til at være 5.51. se vedhæftede billede
Svar #5
29. maj 2017 af janhaa
#4Min lærer har angivet svaret til at være 5.51. se vedhæftede billede
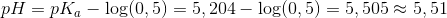
Svar #6
29. maj 2017 af Unintended96 (Slettet)
Hvordan ser reaktionen ud? iforhodl til før(O:) og efter(Eq:) ?
Svar #7
29. maj 2017 af janhaa
#6Hvordan ser reaktionen ud? iforhodl til før(O:) og efter(Eq:) ?
O:
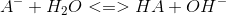
eq:
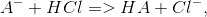
Svar #9
29. maj 2017 af Unintended96 (Slettet)
Altså hvad er reaktionen med de tilhørende M, før og efter?
Skriv et svar til: PH
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.