Kemi
Hjælp til pH-beregning
Hej. Er den nogen der kan hjælpe med den vedhæftede opgave?
Svar #1
16. april 2018 af Heptan
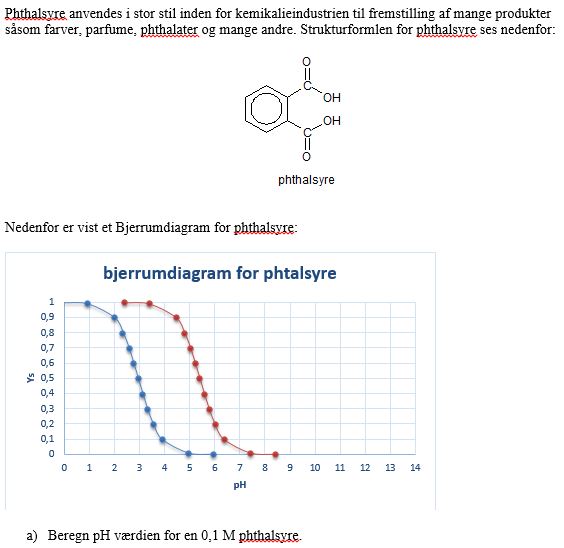
Bjerrumdiagrammet viser at phthalsyre er en divalent syre, dvs. den kan afgive 2 hydroner og der findes 3 former af phthalsyre H2A, HA- og A2-.
På bjerrumdiagrammet kan vi aflæse de 2 pKa værdier for phthalsyre på graferne hvor ys = 0,5. Jeg aflæser pKa1 = 3,0 og pKa2 = 5,4.
Heraf kan vi konkludere at H2A er en middelstærk syre og HA- er en svag syre. Syre/base beregninger for divalente syrer kan være komplicerede, men vi kan lave nogle rimelige antagelser:
1) [A2-] ≈ 0 Den aktuelle koncentration af A2- er så lille at vi ser bort fra den.
2) [OH-] ≈ 0 Den aktuelle koncentration af OH- er så lille at vi ser bort fra den.
Disse antagelser svarer til at vi lader som om at phthalsyre er en middelstærk monovalent syre i en rimelig koncentration. Nu kan vi slå op i formelsamlingen og løse opgaven.
Jeg får pH = 2,0
Skriv et svar til: Hjælp til pH-beregning
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.