Kemi
Bestemmelse af hastighedskonstant og ordre af reaktion.
Jeg har følgende datasæt:
Tid/s: 0,54, 171, 390, 720, 1010, 1190
Absorbans: 1.67, 1.51, 1.24, 0.847, 0.478, 0.301, 0.216
Derved skal jeg bestemme hastighedskonstanten og reaktionsordren.
Hvordan skal denne opgave løses, og gribes an? Håber på jeres hjælp! Tak.
Svar #1
18. september 2018 af swpply (Slettet)
Plot dine data i et (tid, absorbans)-plot og prøv at fitte en eksponentiel udvikling til dette datasæt.
Hvis der er god overensstemmelse imellem fit og data (god R2 værdi) så kan du slutte at du har med en 1st ordens reaktion at gøre. Brug da din viden om 1st ordens reaktioner og værdierne for dinne fit parametere til at bestemme/"aflæse" hastighedskonstanten.
Svar #2
18. september 2018 af swpply (Slettet)
Et godt råd, lad din y-aske være logaritmisk i dit plot. Idet at ekponentielle funktioner er lineære i et sådan enkelt/semi logaritmisk plot.
Svar #3
18. september 2018 af swpply (Slettet)
NB. din opgave er mere kemi orienteret end fysik orienteret.
Svar #4
18. september 2018 af sansas
Jeg har plottet mine dater, hvor tid er på x-aksen og absorbans på y-aksen. Min R2 værdi ligger på: 0,94371
Og ligningen svarer til: y=-0,0012x+1,5038
Hvordan finder man hastighedskonsten udfra ligningen her? Og er det en 1.orden reaktion vi har med at gøre? Hældningen sv.t. -k i det her tilfælde.
Svar #6
18. september 2018 af swpply (Slettet)
#5Kan jeg ændre faget, eller er det forsent?
Nej, men du behøves ikke at ændre faget. Det er bare til en anden god gang ;-)
Har du prøvet at gøre hvad jeg har beskrevet ovenfor ??
Svar #8
18. september 2018 af sansas
Jeg prøver at gøre det logaritmisk, men får fgl. boks fremme:
"Nogle tendenslinjer kan ikke blive beregnet ud fra data, som indeholder negative værdier eller nulværdier."
Svar #9
18. september 2018 af mathon2 (Slettet)
Hvis du uploader alle dine værdier, så kan jeg godt hjælpe dig.
Lige nu er der 6 værdier for tiden, mens der er 7 værdier for absorbans.
Svar #10
18. september 2018 af sansas
Jeg har uploadet alle værdier faktisk, og det er 0 i starten efterfulgt af 54, så 7 værdier i alt. Men jeg vedhæfter dem lige i et billede:
Svar #11
18. september 2018 af mathon2 (Slettet)
Der er tale om en første ordens reaktion, og hastigskonstanten svarer til hældningen
Svar #12
18. september 2018 af mathon2 (Slettet)
Du skal ikke bruge LOG, men LN i stedet.
Dette vil sige, at du tager ln til alle dine værdier for absorbans.
Svar #13
18. september 2018 af swpply (Slettet)
Svar #14
18. september 2018 af sansas
Min excel er gået ned, så kan desværre ikke fortsætte, men ifølge Mathon, så skal man tage ln af absorbansen. Derved kan man plotte ln til absorbansen mod tiden. :-)?
Svar #15
18. september 2018 af swpply (Slettet)
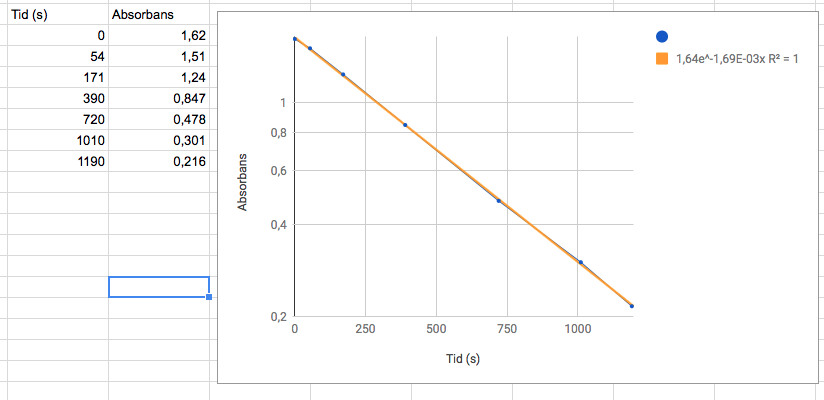
Du finder altså ved fitte en eksponentiel udvikling til dit datasæt, at absorbansen afhænger af tiden på følgende måde
Svar #17
18. september 2018 af swpply (Slettet)
#14Min excel er gået ned, så kan desværre ikke fortsætte, men ifølge Mathon, så skal man tage ln af absorbansen. Derved kan man plotte ln til absorbansen mod tiden. :-)?
Både ja og nej,
Du kan nøjes med at vælge din y-aske til at være logaritmisk.
Svar #18
18. september 2018 af mathon2 (Slettet)
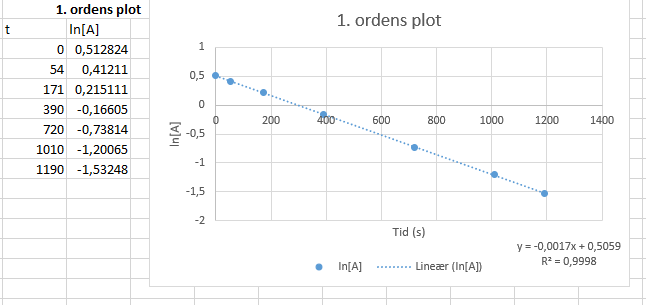
Du kan enten lave en eksponentiel udvikling, eller så kan du tage ln til absorbansen og lave en lineær regression.
I kemi vælger man typisk at lave lineær regressioner, da dette er nemmere og pænere, men begge måder er korrekte.
Svar #19
18. september 2018 af swpply (Slettet)
#18Du kan enten lave en eksponentiel udvikling, eller så kan du tage ln til absorbansen og lave en lineær regression.
I kemi vælger man typisk at lave lineær regressioner, da dette er nemmere og pænere, men begge måder er korrekte.
Begge måder er vel ækvivalente.
Svar #20
18. september 2018 af swpply (Slettet)
OPFØLGNING TIL SVAR #13
Du finder altså ved fitte en eksponentiel udvikling til dit datasæt, at absorbansen afhænger af tiden på følgende måde
Hvor fittet har en R2 = 0.9998.
Brug nu at der gælder følgende sammenhæng imellem absorbans og koncentration :
hvor benævner ekstinktionskoefficienten og
er kuvettebredden. Hvorfor at
Du kan dermed slutte at reaktionen er en 1st ordens reaktion med hastighedskonstant k = 0.00169 1/s.










 .
.