Kemi
Hjælp phosphorsyre
15. januar 2020 af
Lara45
-
Niveau: B-niveau
Hej
Er der en der kan hjælpe mig med nedenstående opgave?
Jeg ved phosphorsyre er en middelstærk syre, men hvilken formel kan jeg bruge til at beregne det?
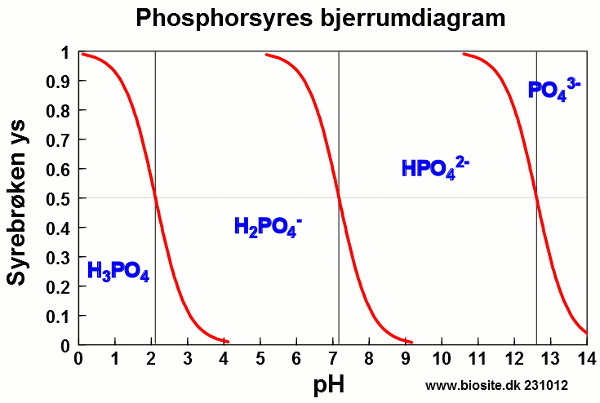
Angiv forholdet mellem de to mest fremherskende syre-base former i en 0,01 M vandig opløsning af phosphorsyre med et pH på 7,21.
Skriv et svar til: Hjælp phosphorsyre
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.