Kemi
Koncentrationsændring
20. januar 2020 af
KFMK
-
Niveau: B-niveau
Jeg har følgende reaktion: Fe^3+ (aq) + SVN^- (aq) <- -> FeSCN^2+ (aq)
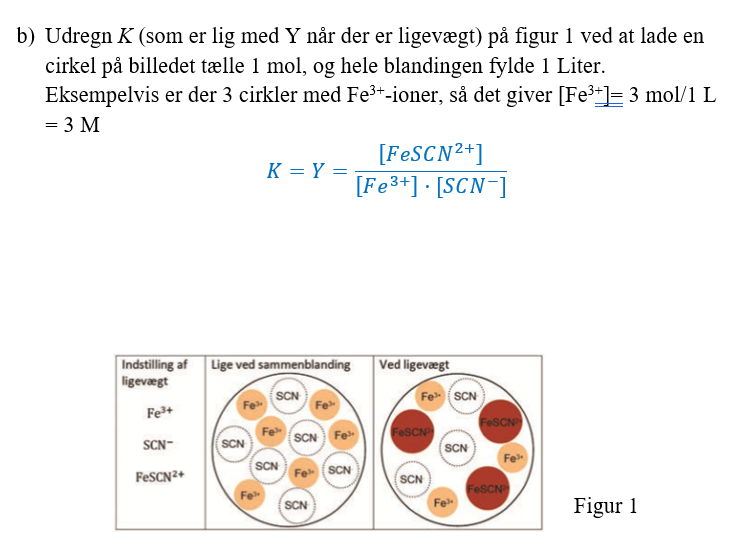
Jeg har opskrevet ligevægtsloven for reaktionen, nu skal jeg udregne K. Her er jeg gået lidt i stå, vedhæftet se opgaven, jeg ved ikke helt hvordan jeg skal gribe den an.
Vedhæftet fil: Udklip.PNG
Skriv et svar til: Koncentrationsændring
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.