Kemi
HJÆLP til pH-beregning
Hej alle,
jeg har siddet fast i denne opgave i en dag nu og kan bare ikke få læst mig frem til hvad, jeg skal gøre...
Jeg er selvstuderende og kan ikke få hjælp andre steder.
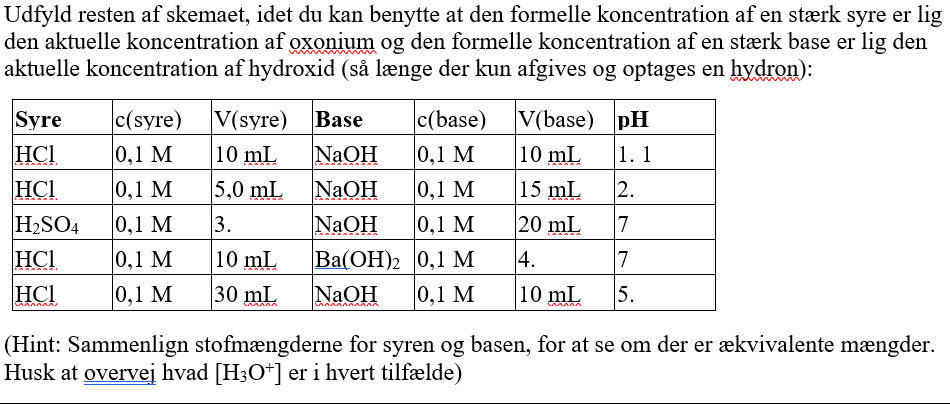
Jeg skal udfylde resten af skemaet.
Jeg ved at pH er -log[H3O+] og at man skal bruge noget n = c*V og V n/c. Jeg kan bare ikke gennemskue metoden trods jeg har læst utallige opslag herinde.
jeg tænker at pH i første række er 1, fordi det er HCl der er den stærke syre så jeg har sagt 0,1 i -log.
I anden række må pH være højere, da V blandingsforholdende er anderledes - men hvilken formel skal jeg bruge for at udregne??
De andre opgaver, hvor jeg skal finde V er jeg også helt tabt på. Det er sikkert noget med ækvivalente mængder, men jeg kan ikke forklare det godt nok.
Håber på nogle, der kan forklare mig hvordan jeg skal gøre!
HCl c: 0,1 M V: 10 mL NaOH c: 0,1 M V: 10 mL pH: ??
HCl c: 0,1 M V: 5 mL NaOH c: 0,1 M V: 15 mL pH: ??
H2SO4 c: 0,1 M V: ?? NaOH c: 0,1 M V 20 mL pH 7
HCl c: 0,1 M V: 10 mL Ba(OH)2 c: 0,1 M V ?? pH: 7
HCl c: 0,1 M V: 30 mL NaOH c: 0,1 M V: 10 mL pH: ?
Svar #1
10. oktober 2021 af Glasurbolle
Til række 2 er det så n(H30+) 0,1 M * 0,005 L = 10-5 og n(NaOH) = 0,1 M * 0,015 L = 1,5* 10-4
pH = -log[H3O+] = -log(10-5) = 5?? :)
Svar #3
10. oktober 2021 af Glasurbolle
I første række pH - den har jeg udfyldt :)
I anden række er det også pH. den er jeg kommet frem til måske er 5
I række 3 V af HCl
I række 4 V af Ba(OH)2
I række 5 pH igen
Svar #4
10. oktober 2021 af Soeffi
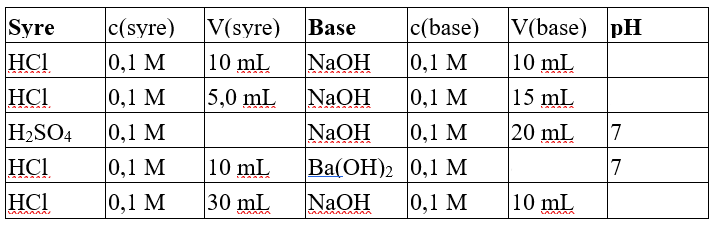
#3. Dvs. man skal udfylde følgende skema: (?)...
Skriv et svar til: HJÆLP til pH-beregning
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.