Kemi
Beregn værdien af ligevægtskonstanten for BaF2
BaF2 er relativt tungtopløselig i vand. I en opløsning af BaF2 i vand ved 25 ºC har vi ved titrering bestemt koncentrationen af Ba2+ til at være 6,3·10-3 M. I kan antage Güntelbergs formel.
1) Opskriv udtrykket og beregn værdien af ligevægtskonstanten for BaF2.
Har opskrevet udtrykket, men kan ikke finde ud af, at beregne værdien af ligevægtskonstanten for BaF2 :-(
Vi blander 100 ml af en 0,3 M NaF opløsning med 100 ml af en 0,15 M BaCl2 opløsning.
2) Beregn ionstyrken af denne blanding. Husk, at BaF2 er tungtopløseligt.
Denne del kan jeg slet ikke finde ud af!
Svar #2
20. januar 2015 af Heptan
2)
Koncentrationerne halveres initialt, derefter fælder bariumfluorid indtil ligevægten er nået. For ændringen x fås
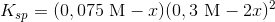
Heraf beregnes de aktuelle koncentrationer:
![[F^-]=0,3\ \textup{M}-2x](https://media.studieportalen.dk/images/equations/QilDYouWFJW22vxPgY6PXg==.gif)
![[Ba^{2+}]=0,075\ \textup{M}-x](https://media.studieportalen.dk/images/equations/Yw0_ZuqhtYB-e2as5CPTOQ==.gif)
Ionstyrken er givet ved
![\mu = \frac{1}{2} \left ([Ba^{2+}]\cdot 2^2+[F^-]+[Na^+]+[Cl^-] \right )](https://media.studieportalen.dk/images/equations/zDHWZlkqybTyfXtRWfaUlA==.gif) jf. biosite.dk
jf. biosite.dk
Svar #4
21. januar 2015 af Silahm (Slettet)
Har fået at vide, at de skal give:
1) = 4,3·10-7
2) = 0,15
Men kan ikke få det til at passe med det du har skrevet...
Skriv et svar til: Beregn værdien af ligevægtskonstanten for BaF2
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.




![K_{sp}=[Ba^{2+}]\cdot [F^-]^2=[Ba^{2+}]\cdot (2\cdot [Ba^{2+}])^2](https://media.studieportalen.dk/images/equations/ZTQ0d0LRVGvGnNMBYnk0NQ==.gif)