Kemi
Kemi om mængdeberegning
Hej nogle som kan hjælpe mig med disse opgaver ::
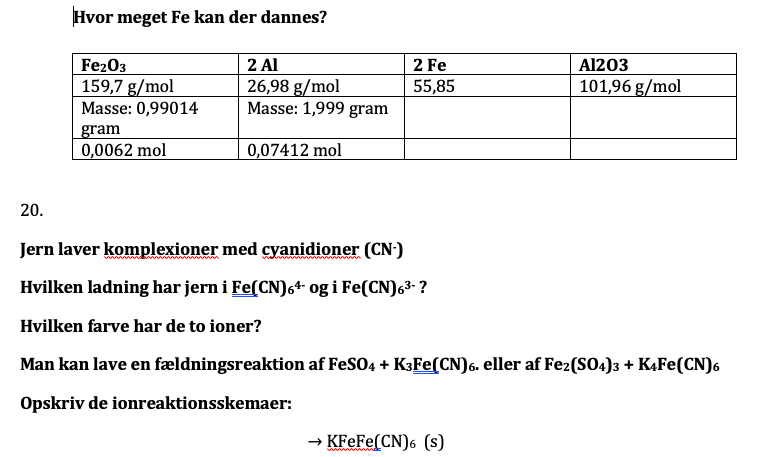
En blanding laves af Fe2O3 og aluminium. Hermed er reaktionen Fe2O3 + 2Al --> 2 Fe + Al2O3
Hvor meget kan Fe der dannes??
Jeg har lavet en mængdeberegningskema som i kan se på det vedhæftet fil.
Desuden ved jeg ikke hvordan jeg skal løse opgave 20 som i kan se på filen.
Håber i vil hjælpe mig :)
Svar #3
22. april 2020 af Soeffi
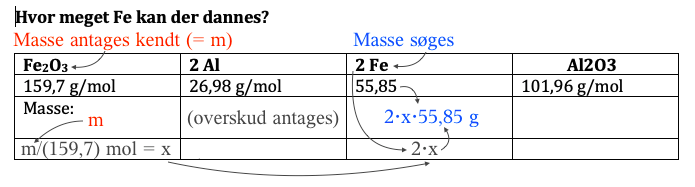
#0. Massen af jern: Jeg er ikke sikker på, hvad der er kendt, og hvad du har beregnet. Jeg antager, at massen af jern(III)oxid er kendt og sætter den til m. Fremgangsmåden er som følger:
Svar #5
22. april 2020 af Soeffi
#3. Hvis vi siger, at begge masser i skemaet er givne i opgaven, så skal vi starte med at finde ud af hvilken reaktant, som er i underskud. Denne beregning er vist nedenunder:
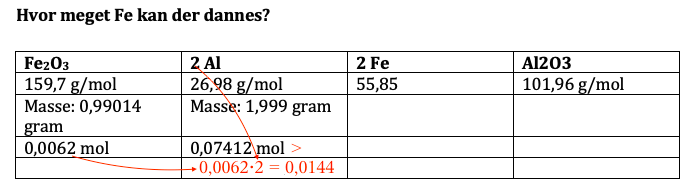
(Hov: 0,0062·2 = 0,0124.)
Da jern(II)oxid er i underskud, så kan alt jern(II)oxid reagere og dermed er beregningen i #3 rigtig.
Hvis aluminiumoxid er i underskud, så kan der dannes lige så mange mol jern, som der er mol aluminiumoxid til at starte med. Dette skyldes, at jern og aluminiumoxid har samme koefficienter i reaktionsskemat og dermed reagerer 1:1.
Svar #7
22. april 2020 af Soeffi
#6. Ja hvis massen af jern(III)oxid er 0,99014 g og massen af Al er 1,999 g.
Lige en rettelse mere:
Hvis aluminium er i underskud, så kan der dannes lige så mange mol jern, som der er mol aluminium til at starte med. Dette skyldes, at jern og aluminium har samme koefficienter i reaktionsskemat og dermed reagerer 1:1.
Skriv et svar til: Kemi om mængdeberegning
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.