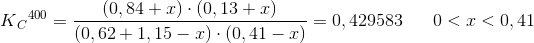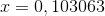Kemi
Ligevægt af gasser
Opgave 3.8
I en beholder findes en ligevægtsblanding af 4 gasser ved 400 K:
SO2 + NO2 <=> SO3 + NO
Beholderen indeholder følgende stofmængder:
n(SO2) = 0,62 mol
n(NO2) = 0,41 mol
n(SO3) = 0,84 mol
n(NO) = 0,13 mol
a) Beregn en værdi for ligevægtskonstanten ved 400 K
(hvorfor behøver vi ikke kende beholderens volumen?)
Her har jeg beregnet en ligevægtskonstant på 0,4295
Uden at ændre temperaturen fyldes nu momentant 1,15 mol SO2 ind i beholderen
b) Beregn en værdi for Y umiddelbart efter tilsætningen og angiv til hvilken side reaktionen forskydes for at genvinde en ny ligevægt.
Introducer en variabel x som forklarer ændringen mod den nye ligevægt og opstil et S-Æ-L system (S = start, Æ = ændring, L = ligevægt)
c) Beregn stofmængderne af alle 4 gasser, når den nye ligevægt er indstillet (stadig 400 K)
Jeg håber der er nogle der vil hjælpe mig med b) og c)
På forhånd tak :)
Svar #1
20. maj 2014 af Heptan
b) Forskydes mod højre
Umiddelbart efter tilsætningen vil der være:
n(SO2) = 0,62 mol + 1,15 mol -x
n(NO2) = 0,41 mol - x
n(SO3) = 0,84 mol + x
n(NO) = 0,13 mol + x
Svar #2
20. maj 2014 af Heptan
Beregn reaktionsbrøken, ved at udelade de x'er jeg har skrevet. Beregn ligevægtskonstanten ved at regne med de x'er jeg har skrevet.
Skriv et svar til: Ligevægt af gasser
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.