Kemi
Kemisk ligevægt
Hej alle,
Nogle som kan hjælpe med flg. opgave:
For ligevægten 2NOBr (g) <-> 2NO (g) + Br2(g) er K = 1,6 * 10-3M ved 25 grader celsius.
0,0200 mol NOBr spærres inde i en beholder med et rumfang på 1,00 L der termostateres ved 25 grader. Beregn koncentrationerne af NOBr, NO og Br2 når ligevægten er indtrådt.
Hvad jeg indtil videre er kommet frem til er, at vi har en startværdi for 2NOBr på 0,0200 mol samt at vi har fået oplyst rumfanget V. Herfra går jeg i stå. Nogle som kan hjælpe?
Svar #1
09. oktober 2016 af mathon
Da volumen er 1,00 L, er volumental og molaritetstal identiske:
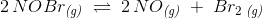
ligevægtsmolariteter: 0,0200 - 2x 2x x
ligevægtsbrøk
![\frac{\left [ NO \right ]^2\cdot \left [ Br_2 \right ]}{ \left [NOBr \right ]^2}=K_c](https://media.studieportalen.dk/images/equations/vZr8JnOqSp6qEk8FGRuHXw==.gif)
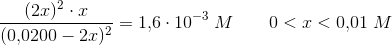
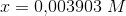
ligevægtsmolariteter: 0,01219 M 0,007807 M 0,003903 M
Svar #2
09. oktober 2016 af hejmeddigvenner (Slettet)
#1Da volumen er 1,00 L, er volumental og molaritetstal identiske:
ligevægtsmolariteter: 0,0200 - 2x 2x xligevægtsbrøk
ligevægtsmolariteter: 0,01219 M 0,007807 M 0,003903 M
Må jeg spørge hvordan du kommer frem til 1,6*10-3? kan ikke få det til det samme på lommeregner
Skriv et svar til: Kemisk ligevægt
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.


