Kemi
Hvor meget masse?
15. december 2016 af
1jazzoz
-
Niveau: A-niveau
I reaktionen AgNo3+Nh4Cl=AgCl+NH4NO3
Der skal vi beregne hvor mange gram AgCl der dannes. Det oplyses at AgNo3 har volume på 31,2 ml og en koncentrtion på 0,5. Tilsvarende har NH4Cl et voumen på 31,0 ml og en koncentration på 0,3.
Den burde ikke være specielt svær, men jeg kan ikke ramme det rigtige resultat som er 1,33g.
Jeg har fundet stofmængden(n) for hvert af de to stoffer og ganget med M for at finde massen der er tilstede af AgNO3 og NH4Cl.
Skriv et svar til: Hvor meget masse?
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.





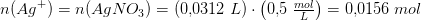
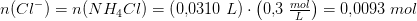 (den
(den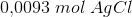 da den opløste mængde kan negligeres
da den opløste mængde kan negligeres