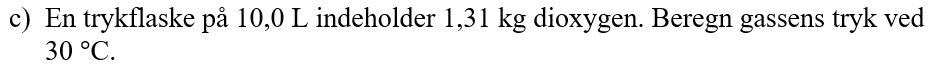Fysik
gas
jeg er lidt i tvivl om hvilken formel jeg skal bruge her min første tanke var idealgasligningen men det kan man vel ikke fordi der ikke er oplyst nogen stofmængde
Svar #1
15. juni 2022 af OliverHviid
Stofmængden kan udregnes som n=m/M hvor n er stofmængden, m er massen og M molarmassen
Svar #2
15. juni 2022 af ikjuijhy
ja men problemet er vi har kun massen oplyst så vi kan heller ikke regne det på den måde
Svar #6
15. juni 2022 af Eksperimentalfysikeren
Stofmængden er givet indirekte. Det er oplyst, at det er 1,31kg dioxygen. Massen er molarmassen gange stofmængden.
Skriv et svar til: gas
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.