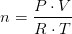Kemi
HASTER… Opg 1. Beregning af mol udfra gasprøve. Opg. 2. Beregning af koncentrationen af OH-
Hjææælp... Jeg har problemer med løsningen af disse 2 opgaver, jeg har svaret på begge men kan ikke komme frem til den rigtige løsning, så håber der er en der kan hjælpe mig med udregningsmetoden :)
Opg. 1.
En gasprøve indeholder 250 mL CO2 ved 760 mmHg, 100 grader celcius. Hvor mange mol CO2 indeholder den??
Svaret = 0,00816 mol
Opg. 2.
Hvis koncentrationen af H3O+ er 3,5 x 10-3 M så er koncentrationen af OH-??
Svaret = 2,9 x 10-12
Svar #5
10. januar 2019 af Lara45
#4 Forstår virkelig ikke, hvordan facit er 0,00816 mol?
Når jeg indsætter alle tal i formlen du skriver for jeg et helt håblst stort tal.
Svar #9
11. januar 2019 af Lara45
#7 Mange tak. Kan du forklare mig, hvordan du omregner gaskonstanten til 62363,669?
Skriv et svar til: HASTER… Opg 1. Beregning af mol udfra gasprøve. Opg. 2. Beregning af koncentrationen af OH-
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.





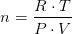
![\left [ OH^-\right ]=\frac{10^{-14}\; M^2}{\left [ H_3O^+ \right ]}](https://media.studieportalen.dk/images/equations/yB1NVlZAIsQ1O7gUiOZAFQ==.gif)