Fysik
Fysik og reaktioner
Ligevægtskonstanten K for reaktioen har værdien 100 ved 20°C og værdien 10 ved 40°C. Ligevægtskonstanten er som sædvanlig defineret som
, hvor [A], [B] og [C] er koncentrationen af molekylerne A, B og C.
Se vedhæftet fil med opgaven
Svar #3
05. januar 2022 af ErDårligTilMat
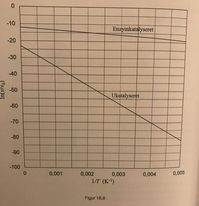
Hov sorry, her er figuren
Svar #5
06. januar 2022 af ErDårligTilMat
her er det i bedre kvalitet, ved ikke hvorfor det blev så dårligt
Svar #7
07. januar 2022 af Heptan
Indsæt formlen for ΔG*:
Dette er forskriften for linjerne. Afmål skæringen og hældningen for hver linje for at beregne ΔH* og ΔS* for hver reaktion.
Svar #8
07. januar 2022 af ErDårligTilMat
Altså har aflæst skæring til at være -23 og hældning til at være -11666
Skal jeg så sigec?
Forstår bare ikke hvordan resten findes...
Svar #9
07. januar 2022 af ErDårligTilMat
Har prøvet noget andet
Har aflæst ln(v/v0) til at være -35 og 1/T til at være 0,001
Og så har jeg indsættet det
Men facit er 98.1*103.....
Svar #11
07. januar 2022 af ErDårligTilMat
Men er stadig forvirret i d)
Man skal beregne ved 4°C og 90°C.
Hvordan beregne man værdien af 1/T ved 4 og 90 grader? Er det bare 1/(273+4)=0,003 og 1/(273+90)=0,002?
Og skal man så aflæse på figuren værdien af ln(vkat/v0) og ln(vukat/v0?)?
Som så er for 0,003: ca. -58 og for 0,002: ca. -47 for ukatalyseret og 0,003: -16 og 0,002: -15 for den katalyseret.
Og så går jeg lidt i stå....
Facit er 7*1020 og 8,7*1016
Svar #12
07. januar 2022 af Heptan
#11 Ja det er korrekt, men tag flere decimaler med. Jeg får fx 1/(273+4) = 0,0036.
Når du har aflæst ln(vkat/v0), så finder du vkat/v0 ved at tage eksponentialfunktionen. Fx:
vkat/v0 = exp( ln(vkat/v0) ) = exp(-58) = e-58
Hvis du aflæser mere præcist, så burde du komme tættere på facit.
Den største brøk har så den største hastighedsforøgelse.
Skriv et svar til: Fysik og reaktioner
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.