Kemi
Ligevægt og tryk
Hej!
Jeg har reaktionen:
N_2 (g) + 3H_2(g) <-> 2NH_3(g) (afstemt)
Jeg skal svare på, hvordan ligevægten påvirkes, når opvarmer reaktionsblandingen ved konstant tryk.
Er der nogen der kan hjælpe med dette?
Derudover søger jeg beskræftelse på, om det jeg har gjort er rigtig i forhold til den førnænvte reaktion:
1. Når der tilsættes N_2(g), vil ligevægten forskydes til højre i reaktionen iflg. Le Chateliers princip
2. Når der tilsættes NH_3(g) vil ligevægten forskydes til venstre i reaktionen -ll-
3. trykforøgelse ved formindskelse af reaktorens rumfang vil medføre, at ligevægten forskydes til venstre i reaktionen.
Eller har jeg byttet om på i hvilken retning forskydelsen sker?
Svar #1
14. september 2017 af mathon
3. trykforøgelse ved formindskelse af reaktorens rumfang vil medføre, at ligevægten forskydes mod højre.
(forskydes mod færrest molekyler)
Svar #2
14. september 2017 af pinklife (Slettet)
#13. trykforøgelse ved formindskelse af reaktorens rumfang vil medføre, at ligevægten forskydes mod højre.
Ah okay! Tusind tak.
Er nr.1 og nr.2 så rigtige?
Svar #4
14. september 2017 af pinklife (Slettet)
#3N2 (g) + 3 H2 (g)
2 NH3 (g) + Q
Hm, jeg forstår ikke helt? Hvad skriver du det i forbindelse med?
Svar #6
14. september 2017 af pinklife (Slettet)
Så det vil sige, at når reaktionsblanden opvarmes ved konstant tryk, så aftager K_c? Så der vil ske en forskydning i den modsatte retning af den exoterme reaktion?
Svar #8
14. september 2017 af mathon
Når reaktionsrummet
hvori processen
N2 (g) + 3 H2 (g) 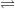 2 NH3 (g) tilføres varme
2 NH3 (g) tilføres varme
vil den oprindelige ligevægt forskydes i den retning, hvor varmeenergi forbruges,
indtil en ny ligevægt er etableret.
Svar #9
15. september 2017 af pinklife (Slettet)
#8Når reaktionsrummet
hvori processen
N2 (g) + 3 H2 (g)2 NH3 (g) tilføres varme
vil den oprindelige ligevægt forskydes i den retning, hvor varmeenergi forbruges,
indtil en ny ligevægt er etableret.
Og hvilken retning er det så? højre eller venstre? Jeg bliver lidt forvirret..
Skriv et svar til: Ligevægt og tryk
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.




