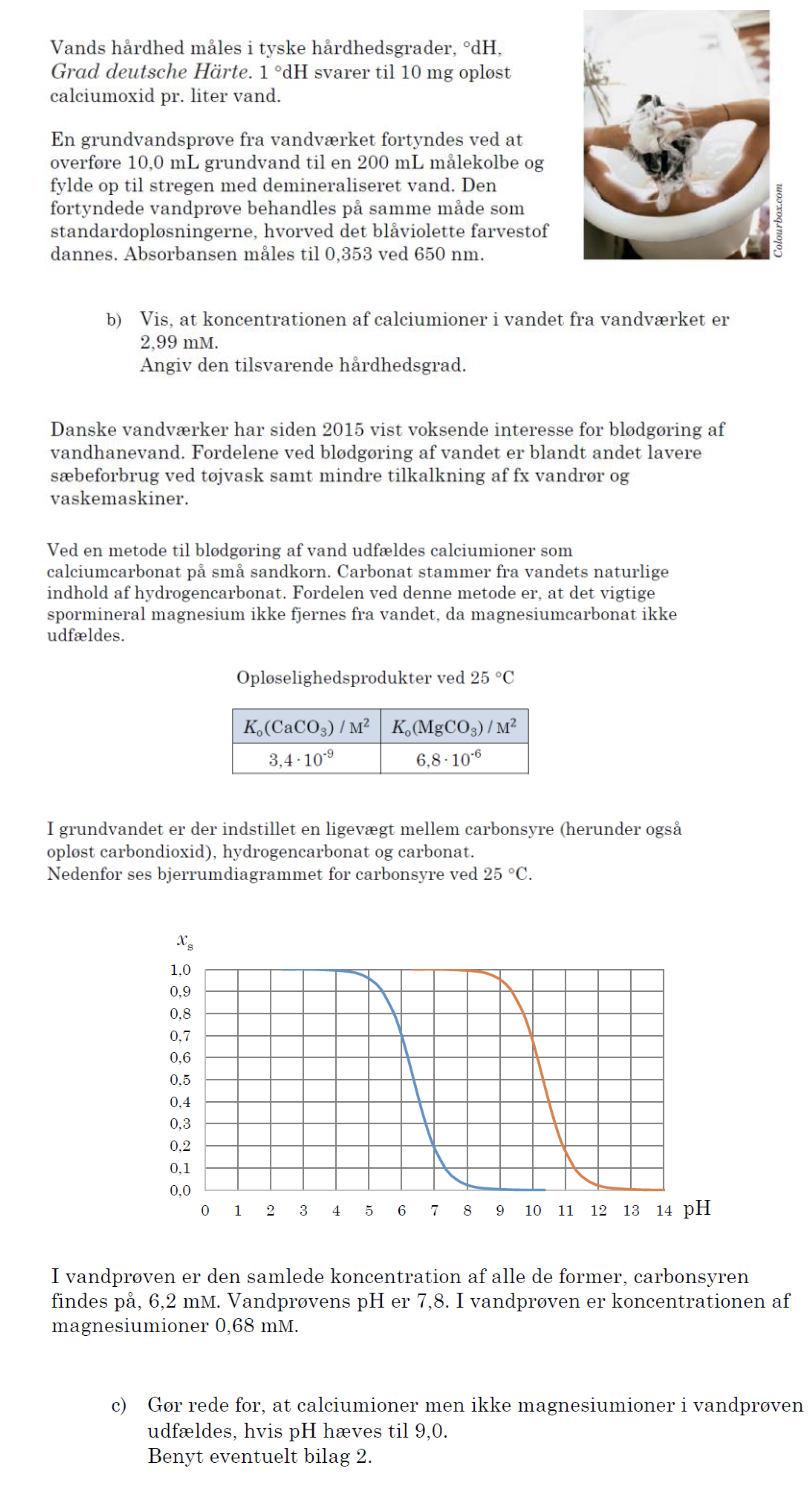
Kemi
Blødgøring af vand
Hej Alle
Håber i kan hjælpe med disse to spørgsmål (har besvaret opg a)
Svar #3
02. januar 2023 af Aktiemester (Slettet)
Den har jeg vedhæftet her
Svar #4
02. januar 2023 af Aktiemester (Slettet)
Jeg får en lineær sammenhæng som er vedhæftet her (svar på spg. a)
Svar #5
03. januar 2023 af Soeffi
#0. b) Koncentration af Ca2+.
Nedenfor er vist en løsning i Geogebra. Den oprindelige koncentration af Ca2+ i vandprøven er 20 gange den i analysen, dvs. 20·0,150 mM = 3,00 mM. (≈ 2,99 mM).
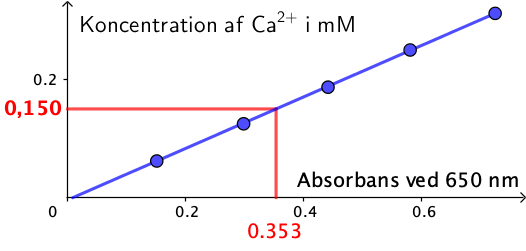
PS: Jeg er usikker på om man evt. skal vælge en linje gennem (0,0) for at få Lambert Beer's lov til at stemme.
Svar #6
03. januar 2023 af Soeffi
#0. b) Hårdhed:
Koncentrationen af Ca2+ i prøven på 2,99 mmol/L ganges med molmasen af CaO, som er 56,0774 mg/mmol, og man får: (2,99 mmol/L)·(56,0774 mg/mmol) = 167,8 mg/L. Dette divideres med 10, og man får hårdheden:
Hårdhed: 17 °dH. (Dvs. Temmelig Hårdt vand, som det kaldes).
Svar #7
03. januar 2023 af Soeffi
#0. c) Man skal sammenligne [Ca2+] og [Mg2+] i vandprøven med ligevægtskoncentrationerne for de to ioner ([Ca2+]eq og [Mg2+]eq) i en mættet opløsning af CaCO3 henholdsvis MgCO3 ved pH = 9,0.
Ligevægtkoncentrationerne findes ud fra opløselighedsprodukterne (K0), den formelle koncentration af kulsyre (c(H2CO3)) og andelen af kulsyre, der er tilstede som CO32- (x i Bjerrumdiagrammet):...
[Ca2+]eq = (K0(CaCO3))/(x(CO32-)·c(H2CO3)) = (3,4·10-9 M2)/(0,05·6,2·10-3 M) = 0,011 mM
[Mg2+]eq = (K0(MgCO3))/(x(CO32-)·c(H2CO3)) = (6,8·10-6 M2)/(0,05·6,2·10-3 M) = 22 mM
Da [Ca2+] (= 2,99 mM) er større end [Ca2+]eq (= 0,011 mM), så fælder CaCO3 ud ved ph = 9,0.
Da [Mg2+] (= 0,68 mM) er mindre end [Mg2+]eq (= 22 mM), så fælder MgCO3 ikke ud ved pH = 9,0.
Svar #8
03. januar 2023 af Aktiemester (Slettet)
#5#0. b) Koncentration af Ca2+.
Nedenfor er vist en løsning i Geogebra. Den oprindelige koncentration af Ca2+ i vandprøven er 20 gange den i analysen, dvs. 20·0,150 mM = 3,00 mM. (≈ 2,99 mM).
PS: Jeg er usikker på om man evt. skal vælge en linje gennem (0,0) for at få Lambert Beer's lov til at stemme.
er det også en mulighed at gøre det på denne måde - ift. at få de 0,150?
Svar #10
03. januar 2023 af Aktiemester (Slettet)
#7#0. c) Man skal sammenligne [Ca2+] og [Mg2+] i vandprøven med ligevægtskoncentrationerne for de to ioner ([Ca2+]eq og [Mg2+]eq) i en mættet opløsning af CaCO3 henholdsvis MgCO3 ved pH = 9,0.
Ligevægtkoncentrationerne findes ud fra opløselighedsprodukterne (K0), den formelle koncentration af kulsyre (c(H2CO3)) og andelen af kulsyre, der er tilstede som CO32- (x i Bjerrumdiagrammet):...
[Ca2+]eq = (K0(CaCO3))/(x(CO32-)·c(H2CO3)) = (3,4·10-9 M2)/(0,05·6,2·10-3 M) = 0,011 mM
[Mg2+]eq = (K0(MgCO3))/(x(CO32-)·c(H2CO3)) = (6,8·10-6 M2)/(0,05·6,2·10-3 M) = 22 mM
Da [Ca2+] (= 2,99 mM) er større end [Ca2+]eq (= 0,011 mM), så fælder CaCO3 ud ved ph = 9,0.
Da [Mg2+] (= 0,68 mM) er mindre end [Mg2+]eq (= 22 mM), så fælder MgCO3 ikke ud ved pH = 9,0.
jeg forstår ikke helt hvor du finder værdierne for formelle koncentration.
andelen af kulsyre, der er tilstede som CO32 - er det bare det 6,2 som du omskriver?
Svar #11
03. januar 2023 af Soeffi
#10...jeg forstår ikke helt hvor du finder værdierne for formelle koncentration...
Den formelle koncentration af kulsyre er givet i opgaven til 6,2 mM (I vandprøven er den samlede koncentration af alle de former, som carbonsyren findes på, 6,2 mM).
...andelen af kulsyre, der er tilstede som CO32- er det bare det 6,2 som du omskriver?
Du har at [H2CO3] + [HCO3-] + [CO32-] = 6,2 mM.
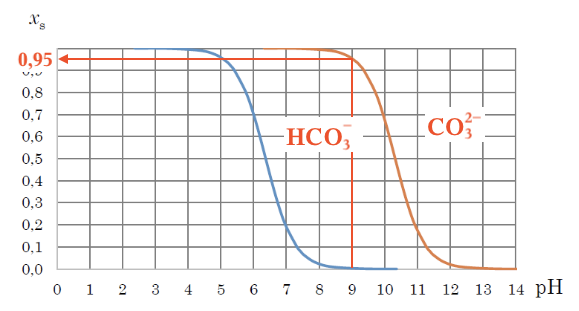
Af Bjerrumdiagrammet fremgår det, at ved pH = 9,0 gælder: [H2CO3] ≈ 0, og derfor at: [HCO3-] + [CO32-] ≈ 6,2 mM. Desuden er xs for HCO3- ≈ 0,95, der aflæses som vist nedenunder.
Man har dermed, at [CO32-] ≈ (1 - 0,95)·6,2 mM = 0,05·6,2 mM = 0,31 mM. Dette tal indsættes i formlerne for opløsningsproduktet.
Svar #14
04. januar 2023 af Aktiemester (Slettet)
#7#0. c) Man skal sammenligne [Ca2+] og [Mg2+] i vandprøven med ligevægtskoncentrationerne for de to ioner ([Ca2+]eq og [Mg2+]eq) i en mættet opløsning af CaCO3 henholdsvis MgCO3 ved pH = 9,0.
Ligevægtkoncentrationerne findes ud fra opløselighedsprodukterne (K0), den formelle koncentration af kulsyre (c(H2CO3)) og andelen af kulsyre, der er tilstede som CO32- (x i Bjerrumdiagrammet):...
[Ca2+]eq = (K0(CaCO3))/(x(CO32-)·c(H2CO3)) = (3,4·10-9 M2)/(0,05·6,2·10-3 M) = 0,011 mM
[Mg2+]eq = (K0(MgCO3))/(x(CO32-)·c(H2CO3)) = (6,8·10-6 M2)/(0,05·6,2·10-3 M) = 22 mM
Da [Ca2+] (= 2,99 mM) er større end [Ca2+]eq (= 0,011 mM), så fælder CaCO3 ud ved ph = 9,0.
Da [Mg2+] (= 0,68 mM) er mindre end [Mg2+]eq (= 22 mM), så fælder MgCO3 ikke ud ved pH = 9,0.
Udfæler magnesium ikke med 0,022 mM i stedet for 22 mM - eller har jeg regnet forkert?
Skriv et svar til: Blødgøring af vand
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.