Kemi
Beregning af opløseligheden
jeg er igang med en opgave om calciumhydroxidphosphat, Ca5(PO4)3OH
Ved opløsning af hydroxyapatit i vand indstiller der sig følgende ligevægt:
Ca5(PO4)3OH (s) ↔ 5Ca2+ (aq) + 3PO43- (aq) + OH- (aq) K0= 10 -36 M9
b) Beregn opløseligheden for calciumhydroxidphosphat. Resultatet angives i mg/L.
man får altså ligevægten
Ca5(PO4)3OH (s) ↔ 5Ca2+ (aq) + 3PO43- (aq) + OH- (aq
ved ligevægt 5x 3x x
og derved fås ligningen 10-36 M-9=(5·x)5·(3·x)3·x
Nu isolerer jeg for x, og får 0,000009 M
Hvilket betyder at opløseligheden for OH er:0,000009 M
For Po: 3*0,000009 M=0,000027 M
For Ca2+:5*0,000009M = 0,000045 M
Jeg kan ikke komme videre, hvad skal jeg gør?
Svar #1
30. maj 2013 af mathon
x betyder den molære vandopløselighed af Ca5(PO4)3OH
M(Ca5(PO4)3OH) = 502,307 g/mol
(10-36 M-9) = (5·x)5·(3·x)3·x
x = 2,836 mol/L
dvs
m/V = (n•M)/V = (n/V) • M = c • M = (2,836 mol/L) • (502,307 g/mol) = 1,424·10-2 g/L = 14,24 mg/L
Svar #3
31. maj 2013 af mathon
(10-36 M9) = (5·x)5•(3·x)3•x
(10-36 M9) = 55•33·x5+3+1
x = ((10-36 M9) / (55•33))1/9
Svar #4
07. november 2015 af Chem5ever (Slettet)
Hej mathon. Hvorfor er eksponenterne blevet lagt sammen i ligning 2 (svar #3)? for når jeg indtaster den første ligning får jeg 2,836*10-5 M
Skriv et svar til: Beregning af opløseligheden
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.




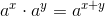 man multiplicerer to potenser med samme rod ved at beholde roden og addere potenseksponenterne
man multiplicerer to potenser med samme rod ved at beholde roden og addere potenseksponenterne