Kemi
Opløselighed og andet
Hej,
Nitrogen har en opløselighed på 5,3·104 M i vand i ligevægt med atmosfæren, hvor partialtrykket af nitrogen er 593 mmHg. Hvad er opløseligheden af ren nitrogen ved samme temperatur, når trykket er 760 mmHg?
- Svaret = 6,8·104 M, men hvordan kommer man frem til det?
Hvor mange gram af fluor (F) er nødvendigt for at producere 20,0 gram FeF3 i den viste reaktion? 2 Fe + 3F2 → 2 FeF3
- Svaret = 10,1 g, men hvordan kommer man frem til det?
Svar #1
30. maj 2015 af mathon
opløseligheden af ren nitrogen ved samme temperatur, når trykket er 760 mm Hg
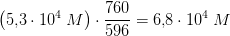 (1 dec.)
(1 dec.)
Svar #3
30. maj 2015 af mathon
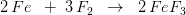
ækvivalente mængder: 3 mol 2 mol
3·(37,996 g) 2·(112,840 g)
113,988 g 225,68 g
x 20,0 g
forholdsberegning:
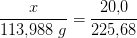
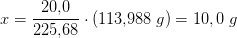
Svar #6
30. maj 2015 af Soeffi
#5 Men i forhold til første spørgsmål er der så en bestemt Formel der bruges ?
Henrys lov.
...Er du sikker på at det ikke er 6,8·10-4 M
Men forstår ikke hvordan det er henrys lov? Er det så Henry konstanten man finder?
Svar #8
30. maj 2015 af Soeffi
Nej Henrys konstant behøver man ikke at kende her. Den er jo bare forholdet mellem koncentrationen af N2 i vand og partialtrykket af N2 i luft. Partialtrykket af N2 i luft er 79% af totaltrykket.
Svar #10
30. maj 2015 af Soeffi
Henrys lov siger, at koncentrationen af N2 i vand er proportionalt med partialtrykket af N2 i atmosfæren. Det er det, som man benytter.
p(N2) = K·c(N2) => p(N2)/c(N2) = K, dvs K = 593 mmHg/5,3·10-4 M = 1.118.897 mmHg/M.
Dette bruges til at finde c = 760 mmHg/(1.118.897 mmHg/M) = 68·10-4 M.
Skriv et svar til: Opløselighed og andet
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.






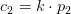
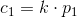
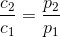
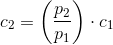
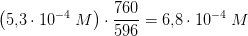 (1 dec.)
(1 dec.)