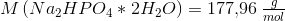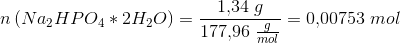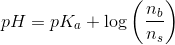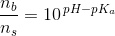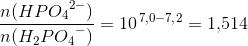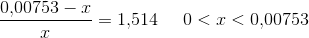Kemi
Eksamensopgave 2015 aug. opgave 4 d
Jeg sidder fast i opgave 4 d, som lyder:
En af opløsningerne indeholder en phosphatpuffer med pH 7,0. Den fremstilles ved først at opløse 1,34 g natriumhydrogenphosphat—vand(1/2) i 50 mL demineraliseret vand i et bægerglas. Derefter tilsættes 0,50 M saltsyre fra burette, indtil pH 7,0. Blandingen overføres kvantitativt til en 100 mL målekolbe, hvorefter der fyldes op med demineraliseret vand til stregen.
- Beregn, hvor stort et volumen af saltsyren der skal tilsættes for at opnå pH 7,0 ved 25 ?C.
Jeg håber på noget hurtigt hjælp.
Svar #3
23. november 2017 af Soeffi
#1
Pufferligningen giver:
Man ved, at antal mol tilsat HCl, nHCl, er lig med både antal mol dannet NaH2PO4- ,ns og antal mol forsvundet base. Dette giver ligningerne: nHCl = ns og nb = 0,00753 - nHCl.
Dette indsættes i pufferligningen:
Man har nu, at CHCl = nHCl/VHCl, hvor man ved, at CHCl = 0,5M , nHCL = 0,004652 mol og ønsker at finde VHCl.
Dette giver VHCl = nHCl/CHCl = 0,004652 mol/(0,5 mol/L) = 0.009304 L = 9,3 mL
Skriv et svar til: Eksamensopgave 2015 aug. opgave 4 d
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.