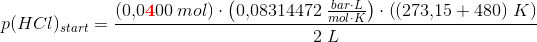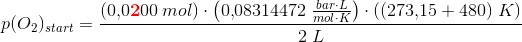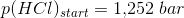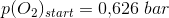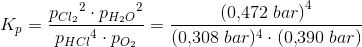Kemi
Beregning af partialtryk og ligevægtskonstant
En beholder med volumen 2,00 dm3 indeholder fra begyndelsen 0,0400 mol HCl og 0,0200 mol oxygen. Ved temperaturen 480 ºC opmåles trykket 1,642 bar efter at følgende ligevægt indstilles:
4 HCl (g) + O2 (g) ⇓ 2 Cl2 (g) + 2 H2O (g) (pilen skal betyde ligevægtspil)
a) Beregn partialtrykket for gasserne ved ligevægt
b) Beregn ligevægtskonstanten for reaktionen
Hvordan gøres dette ? HELP!
Svar #1
21. april 2016 af Heptan
Du skal opstille en ligning for partialtrykkene, idet det totale tryk ved ligevægt er 1,642 bar. Kald en ændring i partialtryk for x.
1,642 bar = (p(HCl)start - 4x) + (p(O2)start - x) + 2x + 2x
Brug idealgasligningen til at bestemme start-partialtrykkene og løs ligningen for x.
Skriv et svar til: Beregning af partialtryk og ligevægtskonstant
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.