Kemi
er der en formel for x?
er vildt forvirret over c) og d)?
Svar #5
25. august 2018 af Lillon (Slettet)

Du skal altså bestemme x i NaxAsOy.
Jeg har lige set, at en anden bruger har allerede stillet spørgsmålet: https://www.studieportalen.dk/forums/Thread.aspx?id=402654
Svar #6
25. august 2018 af hannah9 (Slettet)
n(Na+) = m(Na+)/M(Na+) = (24 · 10-3 g)/(23 g/mol) = 1.04 mmol
er værdi for x så 1.04 mol
Svar #7
26. august 2018 af Lillon (Slettet)
Beregningens sidste trin finder du også på studieportalen: https://www.studieportalen.dk/forums/thread.aspx?id=1768761
Tak til mathon.
Svar #9
26. august 2018 af Lillon (Slettet)
Ja.
Svar 4 af mathon https://www.studieportalen.dk/forums/thread.aspx?id=1768761
Svar #10
26. august 2018 af hannah9 (Slettet)
er det noget med bestemme masseprocenterne eller hva?
Svar #11
27. august 2018 af Lillon (Slettet)
#10
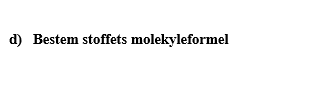
= ”Bestem til sidst værdien for y og angiv stoffets molekyleformel”.
Du har jo bestemt x, nu mangler der kun y, og så har du stoffets molekylformel.
Analyse 1 giver dig stoffets molare masse (opgave b), og analyse 2 giver dig x (opgave c). Altså:
MNaAsOy = MNa + MAs + y*MO = 130,4 g/mol
y = (130,4 g/mol - MNa - MAs)/ Mo
Se også svar 4 af mathon i den anden tråd.
Skriv et svar til: er der en formel for x?
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.





