Kemi
Hvad er den kemiske formel for gær? hjælp haster
Hvad er den kemiske formlen for gær?
Jeg kan simpelhen ikke finde det nogle steder.
Håber en kan hjælpe, da jeg sidder fast i en opgave. På forhånd tak
Svar #1
28. januar 2016 af Arccossintan (Slettet)
Gær er en eukaryot celle, altså ikke et kemisk stof.
Svar #2
28. januar 2016 af annahansen2 (Slettet)
En elev blander i en kolbe 25,0 g glucose, 5 g gær og 250 mL vand. Kolben påsættes et gæringsrør, som tillader CO2, men ikke andet at undslippe. Det hele vejer 367,44 g. Efter tre dage er vægten aftaget til 359,23 g. Hvor mange % af glucosen er forgæret
Så forstår jeg bare ikke, hvordan jeg kan regne opgaven ud. Jeg skal først og fremmest skrive reaktionen op og afstemme den.
Kan du hjælpe mig med denne opgave. Jeg forstår ikke, hvordan, jeg kan skrive reaktionen op uden gær.
HÅber en, kan hjælpe. På forhånd tak
Svar #3
28. januar 2016 af Arccossintan (Slettet)
Dette er reaktionsligningen:
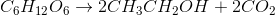
Du finder først differensen mellem kolbens vægt hhv. efter og før reaktionen, altså:
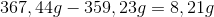
Da der kun slipper CO2 ud af gærrøret, må vægtforskellen være lig med massen af det dannede CO2.
Udregn nu stofmængden af CO2 og derved kan du også udregne massen af glucose og sammenligne massen hhv. før og efter de 3 dage.
Svar #4
28. januar 2016 af Soeffi
#2 Jeg forstår ikke, hvordan, jeg kan skrive reaktionen op uden gær.
Evt.:
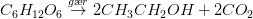
Svar #5
28. januar 2016 af annahansen2 (Slettet)
Stofmængden for CO2: n = m/m --> 8,21/44,01 = 0,1865486. Er det forkert?
Facit siger, at 67,2 % vil være forgæret, men jeg kan simpelthen ikke få det til at gå op.
Svar #6
28. januar 2016 af Arccossintan (Slettet)
Det er den korrekte stofmængde af CO2. Da koefficienten foran glukose er 1, må stofmængden af glukose være halvdelen af stofmængden af CO2 - altså:
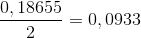
Udregn nu massen af glukose og sammenlign derefter massen af glukose hhv. før og efter gæringen.
Svar #7
28. januar 2016 af annahansen2 (Slettet)
Massen af glukose: m = n *M
m = 2*25g
Jeg svært ved at finde ud af, hvordan jeg kan finde stofmængden for glukose.
Er lidt i tvivl om det jeg gør er rigtigt?
Svar #8
28. januar 2016 af Arccossintan (Slettet)
I dit regnestykke, ganger du den kendte masse, altså massen før reaktionen med stofmængden efter reaktionen. Det går ikke. M, eller Mw, kaldes molarmassen, og denne angiver, hvor mange gram pr. mol et stof vejer. Glukoses molarmasse er 180,1559 g/mol. Du må derfor gange stofmængden (altså 0,0933) med glukoses molarmasse:
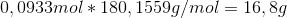
Tilbage står du med spørgsmålet; hvor mange procent udgør 16,8 g af 25 g?
Svar #9
28. januar 2016 af annahansen2 (Slettet)
16,8 /25 *100% = 67,2%. Mange tak for hjælpen.
Jeg har forsøgt at løse nedenstående opgaver, men kan ikke komme videre.
1) Man blander 30 g kobber med 40 g dibrom, og følgende reaktion sker: Cu (s) +Br2 (l)
Hvilket grundstof er den begrænsende faktor? Hvor meget kobber(II)bromid dannes?
Molforholdet er 1:1:
Cu Br2 CuBr2
Stofmængde mol: 1 1 1
molar masse 63,5 79,9 143,4
massen i g 30g 40g
Og herfra kan jeg ikke komme videre :(
2) I 1540 opdager en for os ukendt italiensk alkymist, at bly ved opvarmning i luft øger sin masse med 8-10%. Reaktionsskemaet for reaktionen er: pb (s) + O2 (g) -> PbO (s)
Afstem reaktionsskemaet og beregn, hvor mange gram bly(II)oxid, der dannes ud fra 100 g bly. Kommenter resultatet. IKKE AFSTEMT:Pb(s)+O2 (g)→PbO(s)
Så har jeg afstemt den: 2Pb+O2→2PbO
Men kan ikke komme videre her fra. Gram, der dannes ud fra 100g bly, hvordan beregner jeg det?
Håber virkelig en kan hjælpe mig videre med ovenstående to opgaver. På forhånd tak.
Svar #10
28. januar 2016 af Soeffi
#9 ...Molforholdet er 1:1: 1Cu Br2 CuBr2
molar masse 63,5 g/mol 79,9 g/mol 143,4 g/mol
massen i g 30 g 40 g 0,472 mol · 143,4 g/mol = ...
Stofmængde mol: 0.472 mol 0.501 mol 0,472 mol
Det er rigtigt at molforholdet er 1:1:1, men der er ikke 1 mol af hver af de to reaktanter. Du skal regne ud hvor mange mol der er af hver og derefter finde ud af hvilken reaktant, der er den begrænsende faktor. I dette tilfælde er det Cu, da der kun er 0,472 mol af den og 0,501 mol af Br2. Derfor vil der dannes 0,472 mol CuBr2, mens de 0,472 mol Cu vil reagere med 0,472 mol Br2 og der vil være 0.0286 mol Br2 til overs.
Svar #11
28. januar 2016 af annahansen2 (Slettet)
#10 Mange tak for svar, men hvordan kan jeg beregne, hvor meget kobberbromid, der dannes?
Svar #12
28. januar 2016 af Soeffi
#11 #10 Mange tak for svar, men hvordan kan jeg beregne, hvor meget kobberbromid, der dannes?
Det fremgår af skemaet: 0,472 mol · 143,4 g/mol = 67,7 g (Bemærk: den dannede mængde kan højst være 70 g = 30 g + 40 g i følge loven om massens konstans.)
Svar #13
28. januar 2016 af annahansen2 (Slettet)
#12 Okay tak. Kan du hjælpe med denne sidste opgave, som jeg sidder fast i. Det ville være en kæmpe hjælp.
I 1540 opdager en for os ukendt italiensk alkymist, at bly ved opvarmning i luft øger sin masse med 8-10%. Reaktionsskemaet for reaktionen er: pb (s) + O2 (g) -> PbO (s)
Afstem reaktionsskemaet og beregn, hvor mange gram bly(II)oxid, der dannes ud fra 100 g bly. Kommenter resultatet. IKKE AFSTEMT:Pb(s)+O2 (g)→PbO(s)
Så har jeg afstemt den: 2Pb+O2→2PbO
Men kan ikke komme videre her fra. Gram, der dannes ud fra 100g bly, hvordan beregner jeg det?
På forhånd tak.
Svar #14
28. januar 2016 af Soeffi
#13
2Pb O2 2PbO
molar masse 207,2 g/mol 223,2 g/mol
massen i g 100 g 0,483 mol · 223,2 g/mol = 107,7 g
Stofmængde mol: 0.483 mol 0.483 mol
Bemærk: Det passer nogenlunde med 8%.
Svar #15
28. januar 2016 af annahansen2 (Slettet)
Mange tak Soeffi
Sidste spørgsmål. Jeg mangler hjælp til, inden jeg går i seng :)
Dihydrogen og dioxygen reagerer under dannelse af vand: 2H2O (g) + O2 -> 2H2O (g)
Hvad får man ud af at blande 10 mol dihydrogen med 10 mol dioxygen og antænde reaktionsblandingen udover dårlig hørelse.
Jeg har skrevet at man får dårlig hørelse, men er i tvivl - hvad det er, der eksploderer?
Svar #16
28. januar 2016 af Soeffi
#14 ... Bemærk også, at O2 som regel er i overskud og mængden derfor kan beregnes ud fra Pb, som er den begrænsende faktor
#15 2H2 (g) + O2 (g) -> 2H2O (g)Hvad får man ud af at blande 10 mol dihydrogen med 10 mol dioxygen og antænde reaktionsblandingen udover dårlig hørelse.
Man får 10 mol vand.
Svar #19
28. januar 2016 af Soeffi
#17 hvordan kan du se, at man får 10 mol vand?
O2 er i overskud: af reaktionsskemaet følger, at der kun behøver at være halvt så meget O2 som H2 for at begge dele kan reagere fuldstændigt.
Dvs. H2 bestemmer hvor meget H2O der kan dannes. Der dannes lige så mange mol H2O som der omdannes mol H2 dvs 10 mol.
#18 Hvad er det der eksplodere?
Eksplosionen eller braget skyldes en udvidelse af luften som følge af den varme der opstår ved reaktionen.
Svar #20
01. februar 2016 af lasols (Slettet)
#10 der er vist en lille fejl i beregningen deer er ikke tale om bromradikaler men Br2 som har en molarmasse på 2*79,9=159,8 og dermed briver stofmængden af Br2 0,25mol så det er brom der vliver den begrænsende faktor, princippet er dog rigtigt men du må lige regne tallene igen
Skriv et svar til: Hvad er den kemiske formel for gær? hjælp haster
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.




