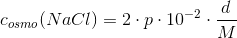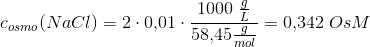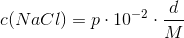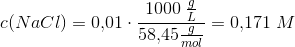Kemi
1% NaCl
Hej venner,
hvordan løser jeg følgende problemstillinger:
1) En 1% NaCl opløsning er det samme som en...
a) 0,171 Osmol/L NaCl opløsning
b) 0,342 Osmol/L NaCl opløsning
c) 0,342 M NaCl opløsning
d) 0,171 M NaCl opløsning
2) En vandig opløsning af ......... er isoton med en osmolaritet på 300 mOsmol/L.
a) 2,75 % glucose
b) 4,5 % glucose
c) 5,4 % glucose
d) 9 % glucose
På forhånd tak :)
Svar #2
28. juli 2016 af mathon
2)
glucose:
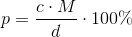 da for glucose:
da for glucose: 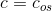
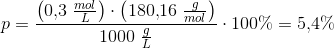
En vandig opløsning af 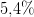 glucose er isoton med en osmolaritet på
glucose er isoton med en osmolaritet på 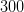 mOsmol/L.
mOsmol/L.
Svar #3
26. december 2016 af pige5 (Slettet)
I forhold til opgave 1, hvor kommer 1000 g/L så fra? :)
Svar #4
26. december 2016 af mathon
#3
Opløsningens densitet er tilnærmelsesvis identisk med vands densistet = 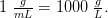
Svar #5
10. august 2019 af Lara45
Jeg sidder med samme opgave.
#1 Hvilken formel bruger du i #1? Er der en simplificeret udgave af den formel som du har skrevet?
Svar #8
15. august 2019 af Lara45
#1 Jeg sidder og prøver at løse samme opgave igen, men jeg kan se, at du har fået 0,171 M NaCl
Hvordan kan det være at facit er 10 g/L NaCl opløsning?
Svar #10
25. december 2019 af N0valyfe (Slettet)
#22)
glucose:
da for glucose:
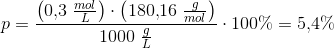
En vandig opløsning af
glucose er isoton med en osmolaritet på
mOsmol/L.
Sidder p.t. med samme opgave - hvorfra får du tallet 1000g/L og 0.3 mol/L?
- Tusinde tak
Skriv et svar til: 1% NaCl
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.