Kemi
Opgave i opgavesæt
Kan nogen forklare hva jeg ska gøre?
Svar #1
13. oktober 2019 af mathon
Undersøg først om én af reaktanterne er i underskud og i givet fald hvilken.
Svar #5
13. oktober 2019 af marielinge
yes, forstår så ikke helt hvad det skal bruges til for at navngive dem?
Svar #8
14. oktober 2019 af Zagoria (Slettet)
Til # 7
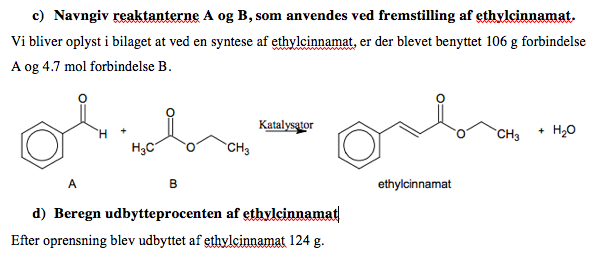
Opgave C:
Reaktant A er et aldehyd , der hedder Benzaldehyd C6H5CHO
Reaktant B er en ester der hedder Ethylacetat CH3COOCH2CH3
Sådan finder du navnet på reaktant A :
Optæl antal C atomer + H atomer + O atomer = C7H6O
Skriv C7H6O i søgefeltet på din computer og gå derefter ind på ChemSpider eller Wikipedia,
der finder du navnet på reaktanten
Svar #9
14. oktober 2019 af Zagoria (Slettet)
#4
Der er 7 C atomer i reaktant A. Men er stadigvæk i underskud.
Skriv et svar til: Opgave i opgavesæt
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.