Kemi
Hvorfor gælder V = 1M / Δt?
Hej,
Jeg har lige et kemi-relateret spørgsmål. Hvis man følger thiosulfate's reaktion med syre kan man opnå dataene på billedet. Hvorfor gælder der, at reaktionshastigheden i dette tilfælde kan beregnes som V = 1M / Δt? Normalt har man jo koncentrationen af et stof i stedet for 1. Kan dette forklares udefra datasættet?
Tak på forhånd!
Svar #1
16. februar 2020 af Heptan
Det lyder også forkert.
Men hvis reaktionen er af nulte orden, kan den beregnes som V = 1/Δt (ingen M),
og hvis den er af første orden, så er V proportional med 1/Δt, så måske er det det de mener.
Se evt https://www.flinnsci.com/api/library/Download/78da6c8204aa48a294bd9a51844543ad
Svar #2
16. februar 2020 af Imagination (Slettet)
Svar #3
16. februar 2020 af Imagination (Slettet)
Svar #4
16. februar 2020 af Heptan
#2 Nej, men skal også bruge koncentrationen for at finde reaktionshastigheden.
#3 Ja, du behøver ikke beregne reaktionshastigheden for at bevise at reaktionen er af 1. orden. Du skal bare plotte 1/Δt som funktion af [S2O3(2-)] ... hvis du får en ret linje, så er reaktionen af 1. orden.
Hvis du synes excel er besværligt, kan du også bare kigge på tallene ... fra forsøg 1 til forsøg 3 fordobles Δt og [S2O3(2-)] halveres, hvilket betyder at reaktionen er af 1. orden.
Svar #5
16. februar 2020 af Imagination (Slettet)
Altså jeg har jo egentlig koncentrationen til givne tidspunkter. Så jeg kan jo godt beregne reaktionshastigheden som funktion af 1/delta t..
Svar #6
16. februar 2020 af Heptan
Ja altså der er ikke noget magisk ved v = 1/delta t, det er bare en anden måde at formulere tiden/reaktionshastigheden på.
Fx hvis det tager 10 min for mig at gå til bageren, så kan jeg gå til:
(1 bager per 10 min).
Reaktionshastigheden er forskellig for hvert forsøg 1,2,3 og 4, fordi koncentrationen er forskellig.
Spørgsmålet er så, hvordan reaktionshastigheden 1/delta t afhænger af koncentrationen [S2O3(2-)], og der kan man lave den graf de også lavede i mit link:
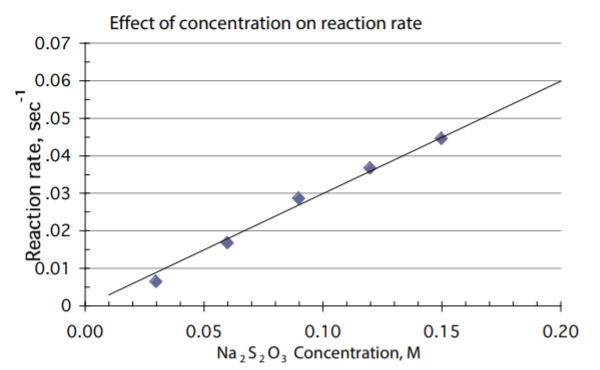
Svar #7
16. februar 2020 af Imagination (Slettet)
Okay det giver lidt mere mening nu. Sorry, jeg er lidt langsom til at forstå tingene. Men Jeg er stadig ikke helt med på, hvordan koncentrationen kommer med ind i billedet. Altså, hvordan kan den overhovedet sættes i relation til, at sætningen v=1/delta t er sand. På din fundne graf er reaktionshastigheden indtegnet som funktion af koncentrationen. Dette er en proportionel funktion. Men hvad siger det om, at v = 1/delta t gælder? Vi har jo ikke en koncentration her.
Da vi fulgte forsøget tilsatte vi syre og thiosulfationer, der dannede frit svovl. I forsøgsbeskrivelsen står der, at man kan udnytte denne til at måle reaktionshastigheden. Så vi måler egentlig, hvor lang tid der går til, at der er dannet en bestemt mængde svovl, der gerne skulle være den samme ved alle de 4 fortaget forsøg. Kunne det måske være pga. at denne er konstant, at man også kan sige v = 1/delta t. Eller er jeg helt galt på den?
Tak for at du gider at tage tid ud til at besvare mine spørgsmål :)
Svar #9
18. februar 2020 af Heptan
Ja hvis der dannes det der svarer til 1 M frit svovl i alle forsøg, så er v = 1 M/delta t.
Ved du hvad den begrænsende faktor er i jeres reaktion? Altså hvilket stof er der relativt mindst af?
Jeg synes bare det er lidt underligt at der fx er tilsat 0,05 M thiosulfat i reaktion 4, og der bliver dannet 1 M svovl, altså hvor kommer svovlen så fra?
Skriv et svar til: Hvorfor gælder V = 1M / Δt?
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.







