Kemi
Le chatelier's princip: Omkring fortynding
Jeg forstår ikke hvordan denne opgave skal løses, nogle der gerne vil hjælpe?
Betragt følgende ligevægtsystem
Fe+3 (aq) + SCN-(aq) <--> FeSCN2+ (aq)
Systemet fortyndes nu til det dobbelte volumen. Herved halveres koncentrationerne
a) Benyt ligevægtsloven til at forklare i hvilken retning reaktionen forskydes ved fortynding. Forklar desuden hvorfor denne forskydning er i overenstemmelse med Le Chateliers princip
Svar #1
18. november 2015 af Toonwire
Opskriv ligevægtsbrøken hhv. før og efter fortynding:
![K_{f\o r}=\frac{[FeSCN^{2+}]}{[Fe^{3+}]\cdot [SCN^-]}](https://media.studieportalen.dk/images/equations/kDRi9Y2STz3NgiY4Y98Hmw==.gif)
![K_{efter}=\frac{\frac{[FeSCN^{2+}]}{2}}{\frac{[Fe^{3+}]}{2}\cdot \frac{[SCN^-]}{2}}=\frac{\frac{[FeSCN^{2+}]}{2}}{\frac{[Fe^{3+}]\cdot [SCN^-]}{4}}\\ \\\\ ~~~~~~~~~~~~~=\frac{[FeSCN^{2+}]}{2}\cdot \frac{4}{[Fe^{3+}]\cdot [SCN^-]} =\frac{4[FeSCN^{2+}]}{2[Fe^{3+}]\cdot [SCN^-]}\\\\\\ ~~~~~~~~~~~~~=\frac{2[FeSCN^{2+}]}{[Fe^{3+}]\cdot [SCN^-]}](https://media.studieportalen.dk/images/equations/hfhUhqLa8Bz66O8M1pp5IA==.gif)
Dvs. den dobbelte koncentration af FeSCN2+ efter fortynding - Retning?
Mht. Le Chateliers princip; hvor stor er koncentrationerne på venstresiden ved fortyndingen (før ligevægten indstilles)?
Svar #2
18. november 2015 af Netcity (Slettet)
Undskyld men jeg har svært ved at forstå svaret, desværre :(
Svar #3
18. november 2015 af Toonwire
#2
En måde at opstille en reaktion er ved reaktionsbrøken, som er lig det der hedder ligevægtskonstanten, 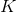 , hvis reaktionen er ved ligevægt.
, hvis reaktionen er ved ligevægt.
Til at starte med har du fået givet en ligevægt:
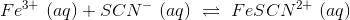
Måden man opstiller denne reaktionsbrøk er ved at have reaktionens produkter i tælleren og reaktionens reaktanter i nævneren. Reaktionsbrøken skrives med symbolet Y.
Disse indgår med deres koncentration hvis der er tale om opløste stoffer (dit tilfælde):
![Y=\frac{[produkter]}{[reaktanter]}=\frac{[FeSCN^{2+}]}{[Fe^{3+}]\cdot [SCN^-]}](https://media.studieportalen.dk/images/equations/jSPQec5X1-NxxE6VeI9DLw==.gif)
Ved en fordobling af voluminet, sker der en forøgelse af af produkt-siden (dobbelt så stor).
Dermed øges ligevægtskonstanten også med en faktor 2.
Le Chateliers princip siger så, at vi skal tilbage til ligevægten og skal derfor modvirke denne indvirkning.
Dvs. reaktionen forskydes mod reaktanterne (altså til venstre)
Skriv et svar til: Le chatelier's princip: Omkring fortynding
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.









