Kemi
Mg^2+ koncentration i vandig opløsning mættet med Mg(OH)2
Nogen der har et bud på hvordan man lige løser den opgave?
Hvad er koncentrationen af Mg^2+ ioner i den mættede opløsning?
Svar #1
21. november 2016 af mathon
I mættet opløsning:
kaldes den molære opløselighed for 
haves:
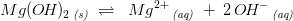
ligevægtsmolariteter: 
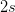
opløselighedsproduktet
er:
![\left [Mg^{2+} \right ]\cdot \left [OH^- \right ]^2=K_{sp}](https://media.studieportalen.dk/images/equations/NttyUwU_oqrJ3pkIQEjyew==.gif)
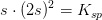
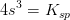
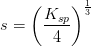
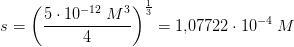
![\left [ Mg^{2+} \right ]_{m\ae ttet}=s=1{,}07722\cdot 10^{-4}\; M](https://media.studieportalen.dk/images/equations/79lS1qB5J_a81ZusuKoOHA==.gif)
Svar #3
21. november 2016 af wes2
Hvorledes har du fundet equilibrium konstanten? På wiki står der, at den er 5.61*10^-4 for magnesium hydroxid. Kan se at svaret skal være [Mg2+] = 1.44*10^-4. Så går ud fra det ikke er den rette værdi af Ksp.
Svar #4
21. november 2016 af mathon
Mit opslag er foretaget i
Tashenbuch der Chemie ISBN: 3-8171-1760-4
men i https://en.wikipedia.org/wiki/Magnesium_hydroxide er Solubility product for Mg(OH)2 opgivet til 5.61×10−12 M3.
Skriv et svar til: Mg^2+ koncentration i vandig opløsning mættet med Mg(OH)2
Du skal være logget ind, for at skrive et svar til dette spørgsmål. Klik her for at logge ind.
Har du ikke en bruger på Studieportalen.dk?
Klik her for at oprette en bruger.







